Septotinia sp.에 의한 개나리 가지마름병(가칭) 발생
First Report on the Shoot Blight Disease of Gaenari (Forsythia koreana) Caused by Septotinia sp. in Korea
Article information
Abstract
이른 봄에 개나리 꽃잎과 잎에 수침상 병반이 나타나서 조직이 괴저하며 마르고 증상이 가지까지 확산되었다. 감염된 가지에는 궤양이 생기며 5월 초부터 윗부분이 말라 죽는데, 가지 기부까지 말라 죽는 경우는 매우 드물었다. 마름 증상을 보이는 가지 조직으로부터 균을 분리하여 병원성을 확인하였다. 대부분의 시료로부터 같은 균이 분리되었는데, potato dextrose agar 배지에서 흰색 균총을 만들었으며 23°C에서 생육이 가장 활발하였고 크기가 다양한 균핵을 많이 만들었다. 개나리의 각 기관에 균사와 균핵 현탁액을 접종한 병원성 검정에서 병원균은 꽃을 감염하며, 잎이나 가지는 감염하지 않는 것으로 나타났다. 꽃에 나타난 증상은 시간이 지남에 따라 잎과 가지로 확산되며 감염 조직을 고사시켰다. 병원균을 동정하기 위하여 ITS, LSU, Tub2, CAL 등 네 가지 유전자의 염기서열을 분석한 결과 Septotinia속으로 동정되었다. 본 연구는 개나리 가지마름병(가칭)에 대한 국내 첫 보고인 동시에 Septotinia속이 식물병원균임을 밝히는 국내 첫 보고이다.
Trans Abstract
In early spring, water-soaked lesions appeared on the petals and leaves of gaenari (Forsythia koreana), and the tissues were necrotic and dry. Cankers appeared on the infected branches around late spring and the above part of a branch withered and died. However, it was very rare that the base of the cankered-branch died. The identical fungi were isolated from the lesions on various tissues, and they grew with white colonies on potato dextrose agar medium. The fungus grew most actively at 23°C and produced many sclerotia of various sizes. In a pathogenicity assay in which mycelial and sclerotial suspensions were inoculated on each organ of forsythia, it was found that the pathogen infects the flower only, but not the leaves or branches. Symptoms on the flowers spread to the next leaves and branches over time and the infected branches were eventually withered. To identify the isolates, DNA sequences of four phylogenetic markers including ITS, LSU, Tub2, and CAL were analyzed and all isolates were identified as a species in the genus Septotinia. This is not only the first report of gaenari (forsythia) shoot blight caused by the fungus Septotinia sp., but also the first report on the genus Septotinia as a plant pathogen in Korea.
서 론
우리나라에서 봄을 알리는 식물로 여겨지고 있는 개나리(Forsythia koreana)는 아시아가 원산지이지만 세계 여러 지역에서 널리 재배되고 있으며, 조경식물로도 인기가 높다. 개나리는 물푸레나무과에 속하는 낙엽성 소교목이며 키가 1−3 m까지 자란다. 줄기는 여러 대가 모여 나며 가지가 많이 갈라져 빽빽하 게 자란다. 잎은 장타원형 또는 주걱모양이고, 꽃은 노란색이며 4월경에 핀다. 열매는 난상 타원형이며 9월에 성숙한다(Kim과 Kim, 2011). 동양에서는 개나리의 열매를 조제한 것을 연교라고 하며 약재로 사용하고 있다. 하지만, 현재 우리나라에서는 개나리를 약제 자원으로 사용하기 보다는 봄철에 꽃을 보기 위한 조경용으로 많이 식재하고 있다. 또한, 일반적으로 환경 적응력이 강하고 병해충과 추위에도 잘 견디는 것으로 알려져 구역 경계를 나타내거나 산울타리를 만드는 등 생활권 녹지 조성에 빠지지 않는 수종이다.
실제로 개나리는 생활권 수종들 중 병 발생이 상대적으로 적 은 수종으로서, 외국에서도 줄기에 만들어지는 작은 혹(Besenyei와 Hevesi, 2003), 뿌리를 제외한 모든 기관을 감염하는 흰가루병(Mieslerová, 2020), 가지나 줄기를 말라 죽게하는 궤양 및 마름병(Daughtrey와 van Broembsen, 2001; He 등, 2023; Hong 등, 2005; Orlikowski와 Ptaszek, 2008), 물관리가 불량한 곳에서 발생하는 뿌리썩음병(Cacciola 등, 1994), 그리고 잎에 기형이나 생육부진을 초래하는 바이러스병(Kaminska, 1985) 등 몇 종류의 병만 보고되어 있을 뿐이다. 현재 우리나라에서 개나리에 발생하는 것으로 보고된 것은 Colletotrichum sp.와 Gloeosporium aridum에 의한 탄저병과 Phyllostica sp.에 의한 점무늬병(Korean Society of Plant Pathology, 2022), 그리고 오이모자이크바이러스(Cucumber mosaic virus)에 의한 바이러스병(Lee 등, 1997) 뿐이다.
최근 몇 년 전부터 개나리 개화기 무렵에 가지의 일부 신초들이 갈색으로 마르며 죽는 현상들이 나타나고 있으며, 심하면 신초가 붙어 있는 가지까지 마름 증상이 번지고 일부가 말라죽기도 하는 등 개나리 생육에 피해를 주고 있다. 따라서 증상을 보이는 가지로부터 균을 분리하여 관찰하고 분자생물학적으로 동정하였으며, 개나리에 접종하여 병원성을 확인하였다.
재료 및 방법
병원균 분리 및 배양
2019년 5월 대전광역시 유성구 가정동 도로변에 산울타리로 심겨진 개나리의 가지와 2020년 3월 청주시 동네 소공원에 조경수로 심겨진 개나리의 신초에서 괴저 및 마름 증상을 관찰하였다.
증상을 보이는 잎과 가지 및 건전해 보이는 잎과 가지를 채집하여 실험실로 운반 즉시 균 분리를 시도하였고, 나머지 시료는 4°C 냉장고에 보관하였다. 균 분리는 증상을 보이는 잎과 가지로부터 Kim 등(2018)에 따라 통상적인 방법으로 수행하였다. 순수분리된 균주들은 단균사분리법으로 시험균주를 확보하고, 균핵, 사면배지 및 멸균수 보관법으로 보관균주를 만들어 상온에 보관하며 이후 모든 연구에 사용하였다.
병원성 검정
개나리 가지마름병균의 병원성을 검정하기 위하여 2019년 7월과 2020년 3월에 충북 청주시 소재 충북대학교 온실과 실험실, 그리고 야외에서 자라고 있는 개나리에 다음과 같은 방법으로 접종하였다. 분리균은 배지에서 균핵은 잘 만들었으나 포자는 잘 만들지 않았으므로 균사현탁액 또는 균핵현탁액을 모두 접종원으로 이용하였으며, potato dextrose agar (PDA) 배지 위에서 자란 균사 또는 균핵을 긁어내어 막자사발에 넣은 다음 멸균수를 첨가하고 곱게 으깨는 방법으로 준비하였다. 균핵은 배지에서 수확 후 4°C에서 10일간 저온처리를 한 후 균사현탁액과 같은 방법으로 준비하였다. 접종원은 개나리의 건전한 잎과 꽃, 가지, 새순 등에 상처접종하였는데, 접종할 자리를 멸균한 바늘로 세 번씩 찔러 상처를 낸 후 20 μl씩 점적하는 방법으로 접종하였다. 병원균을 접종한 개나리와 1 m 이상 떨어져 있는 개나리에는 멸균증류수를 접종원과 똑같은 방법으로 접종하여 대조구로 사용하였다. 검정에 사용한 개나리는 접종 부위에 70% 에탄올을 분무하여 표면소독하였으며, 에탄올이 완전히 마른 후 병원균 마쇄액을 접종하였다.
분리균의 형태적 특성
앞에 설명한 방법으로 분리한 병원균을 PDA 배지에 접종하여 25°C 항온기에서 10일간 배양 후, 분생포자 형성 유무, 생육 특징, 모양, 크기 등 균총의 형태적 특성을 조사하였다. 배지에서 수확한 균핵은 1% glutaraldehyde 에 24시간 이상 고정한 후, Feder와 O'Brien (1968)과 Xing 등(2010)의 방법에 따라 수세, 에탄올시리즈에서 탈수, 파라핀 침투, 포매 과정을 거쳐서 포매블럭을 만들었다. 포매한 균핵은 마이크로톰(Shandon Finesse AS325, Cheshire, UK)을 이용하여 절편을 만들고 safranin O로 염색한 다음 광학현미경(Olympus BX41, Tokyo, Japan)으로 내부 구조를 관찰하였다.
배양온도에 따른 균사생장
순수분리한 병원균 균총의 가장자리에서 cork borer (Φ 6 mm)로 균일하게 떼어낸 균사조각을 PDA 배지에 접종한 후, 17, 20, 23, 27°C 항온기에서 배양하며 일정 간격으로 균총 크기를 버니어캘리퍼로 mm 단위까지 측정하였다. 각 실험은 5회 반복하였다.
또한, 온도에 따른 균핵 형성 능력을 조사하기 위해, 각 배양 온도에서의 균핵 크기와 개수를 조사하였다. 균핵이 완전히 생성된 후 버니어캘리퍼로 균핵 크기를 측정하고 수를 세었다. 자라면서 융합된 균핵은 한 개로 세었다.
Genomic DNA 분리
개나리에서 분리한 병원균 균주들을 PDA 배지에 접종하여 25°C에서 15일간 배양한 후 균사 일부를 떼어내어 ZR Fungal/Bacterial DNA MiniPrep Kit (Zymo Research Co., Irvine, CA, USA)로 DNA를 추출하였다. 추출한 전체 DNA는 –20°C에 보관하며 다음 시험에 사용하였다.
ITS, LSU, Tub2 및 CAL 유전자 영역 PCR 증폭
Internal transcribed spacer (ITS) 1, 5.8S, ITS2 유전자 영역을 증폭하기 위하여 ITS1/ITS4 (White 등, 1990) 프라이머, large subunit rDNA (LSU) 유전자 영역 증폭을 위하여 NL1/LR6 (Fell, 2001; White 등, 1990) 프라이머, beta-tubulin 2 (Tub2) 유전자 일부 영역을 증폭하기 위해 BT2a/BT2b (Glass와 Donaldson, 1995) 프라이머, 그리고 calmodulin (CAL) 유전자 일부 영역 증폭을 위해 CL1C/CL2C (Weir 등, 2012) 프라이머를 이용하였다(Table 1).
PCR 혼합액은 Emerald-Amp GT PCR Master Mix [2× Pre-mix] (Takara Co., Tokyo, Japan)에 전체 DNA를 20−50 ng/μl 넣고, 10 pmole의 양방향 프라이머에 ddH2O를 첨가하여 최종량을 25 μl로 맞추었다. PCR 반응조건은 94°C에서 5분간 denaturation한 후 96°C에서 30초간 denaturation, 그리고 각 프라이머별로 30초간 annealing하고(ITS1/ITS4: 55°C, BT2a/BT2b: 57°C, CL1C/CL2C: 58°C), 72°C에서 1분간 extension을 수행하였는데, 이 과정을 35회 반복하였다. 마지막으로 72°C에서 10분간 extension을 실시하였다. LSU 유전자 영역 PCR 조건은 94°C 에서 2분간 denaturation한 후, 94°C에서 1분간 다시 denaturation, 55°C에서 1분간 annealing, 68°C에서 1분간 extension 하는 과정을 30회 반복하였고, 마지막으로 68°C에서 2분간 extension하였다.
PCR이 끝나면 각 유전자별로 증폭된 PCR 산물 5 μl와 Dyne Loading STAR (Dyne Bio Co., Seongnam, Korea) 1 μl를 혼합하여 1.5% agarose gel에서 100 V로 전기영동을 하고, UV transil-luminator를 사용하여 DNA band 증폭여부를 확인하였다.
염기서열 분석
각 유전자 영역별로 증폭된 PCR 산물은 PCR purification Kit (Bioneer Co., Daejeon, Korea)를 사용해 정제한 후 염기서열 분석기관(Macrogen Co., Seoul, Korea)에 Direct sequencing을 의뢰하였다. 분석된 염기서열은 MEGA 11.0 (Tamura 등, 2021)을 이용하여 오류를 검정한 뒤 연결하였다. 이후 NCBI (National Center for Biotechnology Information, 미국국립생물정보센터)에서 여러 유전자 염기서열과 비교 분석하고, MEGA 11.0 프로그램 내 neighbor-joining meth-od를 사용하여 계통수를 완성하였다.
결 과
감염된 개나리에 나타나는 증상
감염된 개나리는 3월 하순−4월 초순부터 꽃과 신초에서 증상이 나타나기 시작하여 초여름에 전형적인 가지마름 증상을 보였다. 처음에는 한창 자라고 있는 가지 끝 쪽 신초의 꽃과 잎들이 갈색-검은색으로 변하면서 말라 죽었으며, 이러한 증상은 신초 가지로 확산되어 신초 전체가 말라 죽으며 가지로 번져갔다(Fig. 1A, B).

Blight symptoms on flowers, leaves, and twigs of Forsythia koreana. (A, B) Naturally occurred symptoms. (C) Necrosis and wilt of the flowers inoculated with macerated mycelium/sclerotium suspension. (D) Enlargement of a necrotic lesion onto new shoots and a twig. (E) Blighted young twigs. (F) A defoliated and dead twig.
병원균 분리 및 병원성 검정
증상을 보이고 있는 여러 조 직 중 가지에서만 병원균으로 의심되는 균이 분리되었다. 2019년 5월에 대전광역시에서 채집한 병반에서 2균주(CUTP-F001, -F002)와 2020년 3월에 청주시에서 채집한 병반에서 1균주(CUTP-F003) 등 총 3균주를 분리하였는데, PDA 배지에서 모두 같은 특성을 보여 동일한 균으로 생각되었다. 이들은 배지 위에 균핵은 잘 만드는 반면 포자 형성은 매우 적었으므로 단포자 분리 대신 균총 선단부로부터 단균사를 분리하여 각각 표준 균주를 확보하고 증식시키며 이후 시험에 사용하였다.
병원성을 확인하기 위하여 분리균의 균사와 균핵을 막자사발로 으깨어 만든 현탁액을 개나리에 접종한 결과, 온실 접종시험에서는 개나리에 아무런 증상도 나타나지 않았으나 야외에서 자라는 개나리에서는 신초가 괴저되고 마르는 증상이 나타났다. 시기적으로는 온도가 상대적으로 낮은 이른 봄에 접종하였을 때 증상이 잘 나타났으며, 날이 따뜻해진 후에는 증상 발현이 매우 적었다.
또한, 줄기, 잎, 꽃, 눈 등 여러 조직에 접종한 결과, 줄기, 잎, 눈 등에서는 증상이 나타나지 않았던 반면 꽃(화기)에서는 약 10일 정도 지난 후부터 조직이 죽고 시드는 괴저병반이 만들어졌으며(Fig. 1C), 이 병반은 꽃에서 가지(신초)와 잎으로 확산되는 것을 확인하였다(Fig. 1D). 감염된 개나리 꽃에는 흰색 균사들이 보이며 시들기 시작하여 결국 말라 떨어졌으며, 감염된 꽃 근처의 잎들도 점차 마르는 증상을 보였다. 어린잎들은 쳐지는 것을 시작으로 마르고 갈변하였으며, 이러한 증상은 잎자루를 통해 어린 가지로 진전되었다(Fig. 1E). 균을 접종하였던 꽃에서는 균을 재분리하지 못하였으나, 접종한 꽃으로부터 병반이 확산된 가지에서는 균을 재분리할 수 있었으며, PDA 배지에서의 생장 특성과 균총 형태, 균핵 형성 특징 등을 비교하여 접종한 균과 같은 균임을 확인하였다. 감염된 가지가 전체적으로 말라 죽는 경우는 없었지만, 가지 끝부터 20−30 cm 정도까지 마르고 갈변하였으며, 시간이 지나면 잎이 모두 떨어져 그 부분에는 마른 가지만 남았다(Fig. 1F).
병원균 형태적 특성
PDA 배지에서 CUTP-F001, -F002 및 -F003 등 세 균주 모두 연회색 균총을 형성하였으며, 기중균사는 만들지 않았다. 균사가 5일 정도 자랐을 때부터 균핵이 만들어지기 시작하는데, 균총 가장자리와 가운데 부분에서 많이 만들어졌다(Fig. 2A). 어린 균핵은 처음에는 노란 빛을 띄지만, 성숙해질수록 검은색으로 변한다.
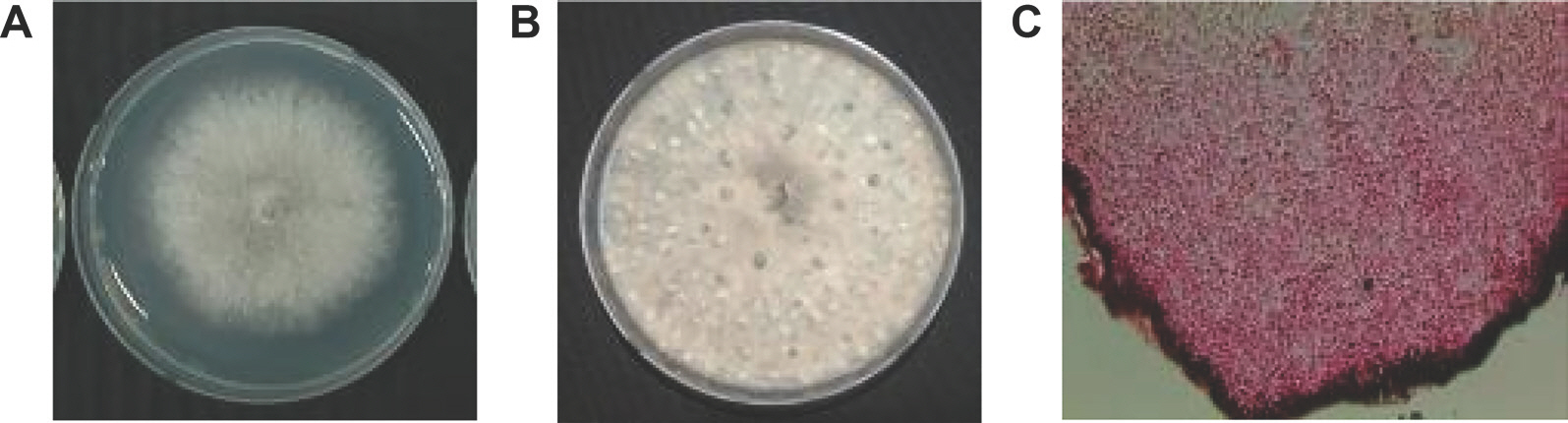
Colony morphology (A) and sclerotia formation (B) of the isolate CUTP-F001 on potato dextrose agar medium and a cross section of a sclerotium (C, ×100).
병원균은 생장 온도에 따라 다른 특성을 보였는데, 23°C에서 자란 균총은 흰색에 가깝고 균핵들이 주로 균총 가운데에 만들어지며 크기는 3−4 mm 정도였다. 병원균을 17°C에서 배양하였을 때는 균총이 회색에 가깝고, 균핵은 주로 균총 가장자리에 만들어지며, 크기도 대개 2 mm 이하로, 23°C에서 배양하였을 때와는 다소 다른 모습을 보였다.
PDA 배지에 만들어진 균핵을 파라핀 포매법을 이용하여 현미경으로 관찰한 결과(Fig. 2B), 수층은 흰색을 띄고 있었고(Fig. 2C는 safranin O로 염색한 것임) 균사가 빽빽하게 존재하여 균사 사이에 공간은 보이지 않았다. 외피는 어두운 갈색 내지 검은색이었다.
배양 온도에 따른 균사 생장과 균핵 형성
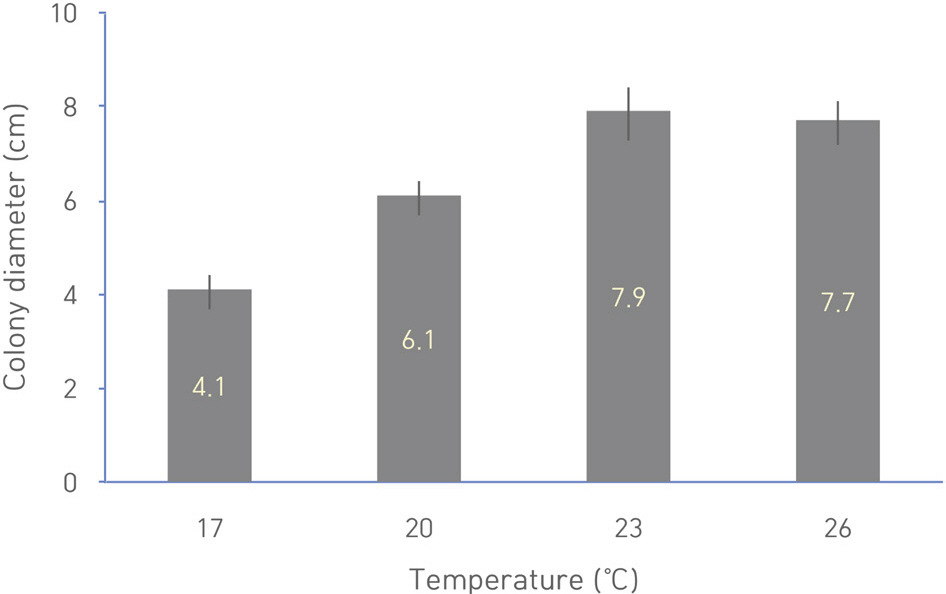
균사 생장을 비교하기 위하여 병원균을 17, 20, 23, 26°C에서 5일 동안 배양한 후 균총의 장축과 단축 길이를 합한 후 평균하였을 때, 17°C에서는 28.1 mm이고, 20°C에서 43.2 mm, 23°C에서 58.3 mm, 26°C에서 57.2 mm로, 23°C에서 균사생장이 가장 활발하였으며 17°C 에서 생육이 가장 느렸다(Fig. 3).
평균 균핵 수는 17°C에서 38.6개, 20°C에서 24.6개, 23°C에서 6개, 26°C에서 13.6개였고, 평균 균핵 크기는 17°C에서 12.6×6.3 mm, 20°C에서 10.9×6.6 mm, 23°C에서 18.0×11.2 mm, 26°C에서 13.6×7.1 mm였다(Table 2). 균핵 수는 23°C에서 가장 적었지만, 크기는 가장 컸다. 23°C에서는 균핵이 균총 가운데에 만들어지고 서로 합쳐져 큰 균핵을 만드는 반면, 17°C에서는 균핵 수는 가장 많지만 크기는 상대적으로 작았다.
병원균의 분자생물학적 동정
개나리에서 분리한 균주 CUTP-F001, -F002 및 -F003의 ITS rDNA, LSU rRNA, partial Tub2 및 partial CAL 유전자 영역에 대한 PCR 결과, ITS 영역은 약 550 bp, LSU는 약 1,300 bp, CAL은 약 820 bp 그리고 Tub2는 약 450 bp 크기에서 각 유전자별로 동일한 PCR산물을 얻었다(Fig. 4).

Agarose gel electrophoresis patterns of PCR-amplified products in ITS, LSU, Tub2 and CAL genes amplified by PCR using primer pairs ITS1/ITS4, NLL/LR6, BT2a/BT2b and CL1C/CL2C. The fungi isolated from blighted shoot of Forsythia koreana in Cheongju and Daejeon. Lanes: 100 bp molecular weight marker (M) and fungal isolates (CUTP-F001, -F002, -F003). PCR, polymerase chain reaction; ITS, internal transcribed spacer; LSU, large subunit rDNA; Tub2, beta-tubulin 2; CAL, calmodulin.
CUTP-F001, -F002, -F003 균주의 ITS, LSU, Tub2, CAL 유전자 염기서열 분석 결과, 세 균주 간에 모든 유전자 염기서열이 100% 상동성을 나타내었으며, 균주 간에 변이는 없었다. CUTP-F001, -F002, -F003 균주의 유전자 염기서열을 NCBI GenBank에 등록하였으며, accession 번호는 다음과 같다: ITS 영역(OR083420−OR083422), LSU 유전자(OR124627− OR124629), Tub2 유전자(OR095783−OR095785), CAL 유전자(OR095786−OR095788).
세 균주의 분자생물적 분류를 위하여 ITS rDNA와 LSU rRNA 유전자 염기서열을 분석한 결과, ITS rDNA 유전자는 GenBank 에 등록된 Septotinia populiperda LS1-5-1 (GenBank accession no. MT093499) 및 S. podophyllina CBS:394.59 (MH857900)와 100% 일치하였다. 다음으로 상동성이 높은 균은 Monilinia속의 M. laxa와 M. fructicola, 그리고 Sclerotinia속의 S. sclerotiorum과 S. trifoliorum 등이었으며 95.5% 이상의 상동성을 나타내었다(Fig. 5A). 따라서 ITS rDNA 영역으로 분석할 때 CUTP-F001, -F002, -F003은 Septotinia속으로 동정되었다.
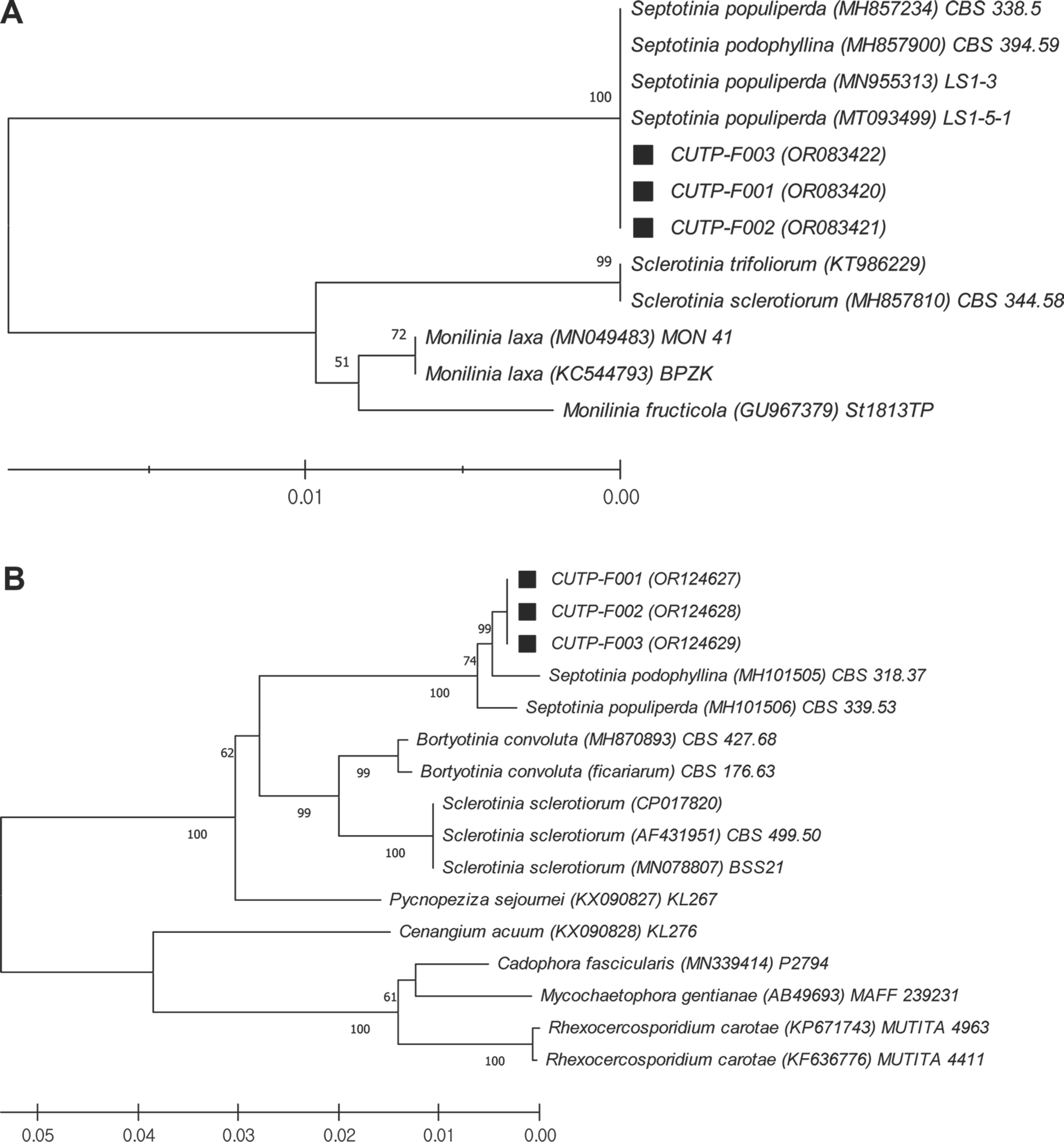
Phylogenetic relationship of the isolates CUTP-F001, -F002, -F003 by partial sequences from ITS rDNA and LSU rRNA regions per-formed with MEGA 11.0 software using the neighbor-joining method. Ten thousand replications for Bootstrap values. (A) ITS rDNA sequences (GenBank accession nos. OR083420−OR083422). (B) LSU rRNA sequences (GenBank accession nos. OR124627−OR124629). ITS, internal transcribed spacer; LSU, large subunit rDNA.
LSU rRNA 유전자 염기서열 역시 Septotinia속과 가장 높은 상동성을 보여, S. populiperda CBS 339.53 (GenBank accession no. MH101506) 및 S. podophyllina CBS:318.37 (MH101505)과 98.7% 이상 일치하였다. Sclerotinia속 S. sclerotiorum, Bortyo-tinia속 B. convoluta, B. ficariarum과의 상동성은 약 93%였다(Fig. 5B). 본 연구의 균주들은 LSU rRNA 유전자 분석에서도 ITS rDNA 유전자 분석과 같이 Septotinia속으로 분류되었다.
Tub2 유전자 염기서열은 GenBank 등록 정보 중 Sclerotiniaceae과에 속하는 Septotinia populiperda (GenBank accession no. QUX37352)를 비롯하여 Sclerotinia sclerotiorum (UQH66463), Botrytis cinerea (ADW7889), Monilinia polystro-ma (WDR20424) 등과 100% 상동성을 나타냈다. 즉, Tub2 유전자는 Sclerotiniaceae과의 속들 간에 변이가 없었으며, 유전적 다양성은 보이지 않았다.
CAL 유전자 염기서열은 세 균주 모두 GenBank에 등록된 Sclerotiniaceae과의 Sclerotinia sclerotiorum (GenBank accession no. CP017814), Botryotis cinerea (XP00155212), Botryotinia tulipae (TGO09976) 등 여러 유전자들과 100% 상동성을 보였 다. 반면, 같은 과에 속하는 Sclerotinia nivalis (GenBank accession no. KAJ8058351), S. trifoliorum (CAD6447131), Botrytis sinoallii (XP038759643), Monilinia laxa (KAB8291167) 등의 유전자와는 상동성이 낮았다. 즉, CAL 유전자에 의한 계통분류는 ITS rDNA 및 LSU rRNA 유전자 계통분류와는 달리 Sclerotiniaceae 일부 속들 안에서도 분자학적 변이가 다양한 것으로 나타났다.
Septotinia sp.의 CAL 유전자 염기서열은 GenBank에 등록되어 있지 않아 본 균주들과 Septotinia sp.와의 상동성은 비교할 수 없었다. 본 연구에서 분리한 CUTP-F001, -F002, -F003 균주의 CAL 유전자 염기서열은 NCBI GenBank에 최초 등록하였다.
즉, 개나리에서 분리한 균주 CUTP-F001, -F002, -F003의 ITS rDNA, LSU rRNA, Tub2 및 CAL 유전자 염기서열을 분석한 결과, ITS rDNA와 LSU rRNA 유전자에서는 Septotinia sp.로 분류되었다. Tub2 유전자는 Sclerotiniaceae의 속들 사이에 변이가 없이 100% 상동성을 보여 속 구분이 불가능했으며, CAL 유전자는 Botrytis속 일부 종들과 100% 상동성을 나타냈으나 Botrytis속의 다른 종이나, Sclerotinia nivalis 등과는 상동성이 낮아 다른 계통으로 분류되었다.
고 찰
개나리 가지마름병(가칭)은 우리나라에서는 아직까지 정식으로 보고된 바 없으나, 병원균은 이른 봄, 개나리 개화기에 꽃을 감염하여 수침상 괴저병반을 만들고 주변 조직으로 확산하며 잎과 잔가지에 괴저와 마름 증상을 일으킨다. 감염된 잎들이 모두 말라 떨어지는 4월 하순 이후에는 감염된 가지에 궤양이 나타나며 마르기 시작하는데, 가지마름이 줄기 기부까지 진전되는 경우는 매우 드물다.
가지마름병은 외국에서는 개나리에 흔히 나타나는 병으로 이미 잘 알려져 있다. 가지마름 증상의 원인으로는 Phytophthora spp., Botryoshpaeria sp., Phomopsis sp. 등 몇 종이 알려져 있는데, 기주에 침입하면 잎이 갈색으로 변하고 시들며, 이러한 증상이 가지로 번져가는 등 매우 비슷한 증상들을 일으킨다(He 등, 2023). 이 중 가장 흔히 거론되는 것이 Sclerotinia sclerotiorum과 Phytophthora nicotianae 등인데, Phytophthora spp.는 감염된 개체의 줄기 기부까지 갈변하며 뿌리에도 괴저가 확산되는 등 본 연구에서 관찰한 결과와는 다른 양상을 보이는 것으로 알려져 있다(Orlikowski와 Ptaszek, 2008). 반면, S. sclerotiorum은 이른 봄에 꽃잎과 잎에 수침상 병반을 일으키는데, 증상이 진전되면서 가지까지 확산되어 가지가 마르는 등 본 연구의 증상과 매우 비슷한 것으로 보고되어 있다(Florea 등, 2022).
Sclerotinia는 생육적온이 20−25°C이며, 0−25°C 범위에서 감수성 기주들을 감염할 수 있는데, 가장 활발하게 감염하는 온도는 15−20°C로 알려져 있다(Chupp과 Sherf, 1960). 또한 이 곰팡이들의 균핵은 표면이 어두운 색 껍질(rind)로 둘러싸여 있으며, 그 안쪽으로 얇은 피층(cortex)이 있고 내부는 위유조직성 수(medulla)로 채워져 있다(Willetts와 Wong, 1980). 본 연구에서 분리한 개나리 가지마름병균도 기온이 낮은 이른 봄에 주로 꽃(화기)을 통해 감염하는 것을 확인하였으며, 분리한 균주들은 23°C에서 가장 빠르게 생육하고 균핵도 잘 만들었다. 병원성 검정에서도 잎이나 가지보다는 꽃에 접종하였을 때 감염이 되었고, 이른 봄에 접종이 잘되는 등 Sclerotinia sp.와 매우 비슷한 특성을 보였다. 하지만 균핵을 잘라 보았을 때 껍질과 수는 있으나 피층은 관찰할 수 없었다.
특히 유전자 염기서열 분석에서 Sclerotinia속보다는 Septotinia속과 상동성이 더 높은 것으로 나타났다. ITS 유전자 등 네 가지 유전자 염기서열을 분석한 결과, ITS 염기서열 분석에서는 Septotinia populiperda, S. podophyllina와 100% 일치함을 보인 반면 Sclerotinia spp., Monillinia spp. 등과는 95% 정도의 상동성을 보였다. LSU 유전자 염기서열에서는 Septotinia spp.와 완전 일치하지는 않았으나 Sclerotinia spp.나 Botryotinia spp.보다는 높은 상동성을 보였다. CAL 유전자 염기서열에서는 같은 속의 균주들 간에도 상동성이 다르게 나타나는 등 종간 변이가 심했다. Tub2 유전자는 Sclerotiniaceae과의 모든 속 간에 차이가 없었다. 즉, 네 유전자 중 ITS와 LSU 유전자가 유의적 결과를 보여주는데, 이 두 유전자에서 모두 Septotinia속이 가장 높은 상동성을 보였으므로 개나리 가지마름 증상에서 분리한 균들은 Septotinia sp.로 동정하는 것이 타당하다고 생각한다. 이러한 결과는 본 연구와 같은 증상을 보이는 개나리를 연구하여 Sclerotinia를 병원균으로 보고한 Florea 등(2022)의 연구와는 부합하지 않으나, 이들은 균을 동정할 때 ribosomal DNA 유전자 한 가지만 확인하였기 때문일 가능성이 크다. Sclerotinia와 Sclerotinia속은 모두 Sclerotiniaceae과에 속하며, 균학적으로도 매우 특성들을 공유하고 있으므로 정확한 동정을 위해서는 여러 유전자를 분석하여야 할 것이다.
본 연구에서 병원균으로 동정된 Septotinia속은 식물병원균으로는 널리 알려져 있지 않으나, S. populiperda는 오래 전부터 Populus속과 Salix속 수목에 잎마름과 가지마름을 일으키는 병원균으로 보고되어 왔으며(Sutton, 1980; Waterman과 Cash, 1950; Zhu 등, 2019, 2022), 최근에는 감자에서도 발생이 보고되었다(Chudinova와 Elansky, 2021). Zhu 등(2022)은 수양버들에 잎마름병을 일으키는 S. populiperda에 대한 연구에서 5균주 중 세 균주만이 유성세대인 자낭반을 형성하였다고 하였다. 또한, 잎에 접종한 10균주 모두 뚜렷한 병반 형성을 유도하였으나 그중 6균주만이 분생포자를 많이 형성하였을 뿐, 2균주는 형성량이 매우 적었고 다른 2균주는 분생포자를 전혀 만들지 않았다고 보고하였으므로, S. populiperda는 균주에 따라 생장 특성에 차이가 크다고 할 수 있다. 본 연구의 균주들은 모두 분생포자 형성률이 매우 낮았으나, 이는 3균주만을 확인한 것이므로 분생포자 형성 여부를 확인하기 위해서는 더 많은 균주를 조사하여야 할 것으로 생각한다. 한편 메이애플(Podophyllum peltatum)에 가지마름병을 일으키는 것으로 알려진 S. podophyllina에 대해서는 S. populiperda와 같은 종이라는 주장이 오래 전부터 제기되어 오고 있다(van den Ende, 1960). 하지만, 본 연구의 계통수 분석에서 S. podophyllina의 ITS rDNA 영역 염기 서열은 S. populiperda와 일치한 반면, LSU rRNA 유전자 염기서열은 완전히 일치하지는 않았으므로(Fig. 5) 두 종이 다를 가능성도 배제할 수는 없다.
Septotinia sp.가 우리나라에서 식물병원균으로 보고되어 있는 것은 Septotinia populiperda 단 1종뿐으로(Korean Society of Plant Pathology, 2022), 같은 시기에 두 건이 보고되어 있다(Byun 등, 1967; Park, 1967). 그러나 Byun 등(1967)의 연구는 ‘산림병해충 발생 조사’에 대한 것으로서 본문에는 포플러에서 S. populiperda에 의한 잎마름병 피해도만 기록되어 있다. Park (1967)의 연구도 ‘국내식물병 발생 조사’로서 본문에는 Populus 속에 발생하는 잎마름병의 원인으로 S. populiperda라는 균 이름만 기재하고 있을 뿐, 국내에서는 Septotinia sp.의 특성에 대한 설명이나 그것이 일으키는 병에 대한 언급은 전혀 없다.
본 연구에서는 마름 증상을 보이는 개나리 가지로부터 균을 분리하였고, 배양 특성과 유전자 염기서열 분석을 통해 Septotinia sp.로 동정하였으며, 접종과 재분리 시험으로 병원성을 확인하였다. 이 결과는 개나리 가지마름병에 관한 국내 첫 진단인 동시에 Septotinia sp.가 식물병원균임을 밝히는 국내 첫 보고이다.
Notes
Conflicts of Interest
No potential conflict of interest relevant to this article was reported.
Acknolwledgments
This work was supported by the research grant of the Chungbuk National University in 2022.