|
 |
| Res. Plant Dis > Volume 26(3); 2020 > Article |
|
ABSTRACT
In July 2018, a serious rust symptom was found throughout the fringe trees planted in Gangjin-gun, Korea. Yellow and brown spots were observed on the adaxial (topside) surface of the collected fringe tree leaves, and yellow color aecia were observed on the abaxial (underside) surface leaves. The size of aeciospore and urediniospores of JCK-KCFR1 strain were measured to 41.2 ╬╝m (╬”) and 28.84 ╬╝m (╬”) with a light microscope. Phylogenetic analysis of the small subunit rRNA, internal transcribed spacer, and large subunit rRNA region indicated that JCK-KCFR1 strain is novel species of the genus Puccinia and closely related to Puccinia kusanoi, which has been reported a rust pathogen on bamboo. In May 2019, rust symptoms were also discovered on the bamboo leaves planted around the fringe tree on Muwisa-ro, and their telia and teliospores were observed on the abaxial leaf surfaces of the bamboo with 100% sequence homology with the rust of the fringe tree. This is the first report that Puccinia sp. JCK-KCFR1 is a new species that requires both primary (fringe tree) and alternative (bamboo) host plants to complete its life cycle in Korea.
ņØ┤ĒīØļéśļ¼┤(Chionanthus retusus Lindley)ļŖö ļ¼╝ĒæĖļĀłļéśļ¼┤Ļ│╝(Oleaceae)ņŚÉ ņåŹĒĢśļŖö ļŗżļģäņāØ ļéÖņŚĮĻĄÉļ¬®ņ£╝ļĪ£ ņØ┤ļ¬ģņ£╝ļĪ£ļŖö ļŗłņĢöļéśļ¼┤, ļŗżņŚĮņłś, ļźśņłśņłś, ņÜ░ĻĘ╝ņ×É, ņ£ĪļÅäļ¬®, ņĪ░ĻĖłņ×É, ļ╗Żļéśļ¼┤ ļō▒ņØ┤ ņ׳ļŗż. ņīŹļ¢Īņ×ÄņŗØļ¼╝ņØĖ ņØ┤ĒīØļéśļ¼┤ņØś ņŗØļ¼╝ļ¬ģņØĆ 5-6ņøöņŚÉ Ļ░£ĒÖöĒĢśļŖö ņØ┤ĒīØļéśļ¼┤ņØś ĻĮāņØ┤ ņīĆļ░źĻ│╝ Ļ░Öļŗż ĒĢśņŚ¼ ŌĆśņØ┤ļ░źļéśļ¼┤ŌĆÖņŚÉņä£ ņØ┤ĒīØļéśļ¼┤ļØ╝Ļ│Ā ļ¬ģļ¬ģĒĢśĻ▓ī ļÉśņŚłļŗżĻ│Ā ĒĢ£ļŗż. ņ×ÄņØĆ ļīĆņāØņ£╝ļĪ£ ļé£ĒśĢ, ĒāĆņøÉĒśĢ, ļśÉļŖö ļÅäļ×ĆĒśĢņØ┤ļ®░ ņŚĮņĀĆļŖö ļæöĒĢśļ®░ ņ×Äņ×ÉļŻ©Ļ░Ć ĻĖĖļŗż. ĒāĆņøÉĒśĢņØś ņŚ┤ļ¦żļŖö 9-10ņøöņŚÉ ņä▒ņłÖļÉśļ®░ ĒØæļ▓ĮņāēņØä ļØżļŗż. ņśłļĪ£ļČĆĒä░ ļ»╝Ļ░äņŚÉņä£ļŖö ņØ┤ĒīØļéśļ¼┤ ņóģņ×ÉļŖö ņäżņé¼ļź╝ ļ®łņČöļ®░, ņ£äņןņØä ĒŖ╝ĒŖ╝ĒĢśĻ▓ī ĒĢśļŖö Ļ▒┤ņ£äņ×æņÜ®ņØ┤ ņ׳ņ¢┤ Ļ░ĢņןņĀ£ļéśņ¦Ćņé¼ņĀ£ļĪ£ ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░, ĒĢ┤ņŚ┤ņĀ£ ļ░Å ņżæĒÆŹ ļō▒ņØś ņ¦łĒÖśņ╣śļŻīņĀ£ļĪ£ļÅä ņé¼ņÜ®ĒĢśņśĆļŗż. ļśÉĒĢ£ ņØ┤ĒīØļéśļ¼┤ņØś ņ¢┤ļ”░ņ×ÄņØĆ ņ░©ļĪ£ ļ¦łņŗ£Ļ▒░ļéś ļéśļ¼╝ļĪ£ ļ¼┤ņ│ÉņĀĖ ņŗØņÜ®ĒĢśĻĖ░ļÅä ĒĢśņśĆļŗż. Ļ┤ĆņāüņĀü Ļ░Ćņ╣śĻ░Ć ļåÆņØĆ ņØ┤ĒīØļéśļ¼┤ļŖöņĄ£ĻĘ╝ņŚÉļŖö Ļ░ĆļĪ£ņłś ļ░Å ņĪ░Ļ▓ĮņÜ®ņ£╝ļĪ£ļÅä ļ¦ÄņØ┤ ņé¼ņÜ®ĒĢśĻ│Ā ņ׳ļŗż. ņé░ļ”╝ņ▓Łņ×ÉļŻīņŚÉ ļö░ļź┤ļ®┤ 2018ļģä ļ¦É ĻĖ░ņżĆ, ņØ┤ĒīØļéśļ¼┤ļŖö ņÜ░ļ”¼ļéśļØ╝ ņ┤Ø Ļ░ĆļĪ£ņłś8,230ņ▓£ļ│Ė ņżæ 608ņ▓£ļ│Ė(7.4%)ņØä ņ░©ņ¦ĆĒĢśņŚ¼ 3ļīĆ Ļ░ĆļĪ£ņłśņóģ ņżæ ĒĢśļéśļĪ£ļÅä ņĢīļĀżņĀĖ ņ׳ļŗż(Korea Forest Service, 2019).
ĒĢśņ¦Ćļ¦ī ņ¦Ćļé£ ļ¬ć ļģä ļÅÖņĢł ņĀäļØ╝ļé©ļÅä Ļ░Ģņ¦äĻĄ░ ņä▒ņĀäļ®┤ ļ¼┤ņ£äņé¼ļĪ£ņŚÉ Ļ░ĆļĪ£ņłśļĪ£ ņŗØņ×¼ļÉ£ ņØ┤ĒīØļéśļ¼┤ļź╝ ĒżĒĢ©ĒĢ£ ņŚ¼ļ¤¼ ņ¦ĆņŚŁņØś Ļ░ĆļĪ£ņłśņÜ® ņØ┤ĒīØļéśļ¼┤ ņ×ÄĻ│╝ ņżäĻĖ░ņŚÉ ļģĖļ׌Ļ│Ā ļ╣©Ļ░ä ļ░śņĀÉņØ┤ ņāØĻĖ░ļ®░ ļ¦ÉļØ╝ņŻĮļŖö ļģ╣ļ│æ
ņØ┤ļīĆļīĆņĀüņ£╝ļĪ£ ļ░£ņāØĒĢśņŚ¼ ņŗ¼Ļ░üĒĢśĻ▓ī Ļ▓ĮĻ┤ĆņØä ĒĢ┤ņ╣śĻ│Ā, ņĪ░ĻĖ░ļéÖņŚĮņØ┤ĒÖĢņé░ļÉśņ¢┤ Ļ░ĆļĪ£ņłśļĪ£ņä£ņØś ņØ┤ĒīØļéśļ¼┤ Ļ░Ćņ╣śļź╝ ņĀÉņĀÉ ĒĢśļØĮņŗ£ĒéżĻ│Ā ņ׳ļŗż. ļīĆļČĆļČäņØś ļģ╣ļ│æĻĘĀļōżņØĆ ņāØĒÖ£ņé¼ļź╝ ņÖäņä▒ĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ņä£ļĪ£ ļŗżļźĖļæÉ ņóģņØś ņŗØļ¼╝ņØä ĻĖ░ņŻ╝ļĪ£ ĒĢäņÜöļĪ£ĒĢ£ļŗż. ņׯļéśļ¼┤ ĒäĖļģ╣ļ│æņØś Ļ▓ĮņÜ░ ļģ╣ļ│æĒżņ×ÉņÖĆ ļģ╣Ēżņ×ÉņäĖļīĆļź╝ ņׯļéśļ¼┤ņŚÉņä£ ļ│┤ļé┤Ļ│Ā, ņåĪņØ┤ĒÆĆĻ│╝ Ļ╣īņ╣śļ░źļéśļ¼┤ņŚÉņä£ ņŚ¼ļ”äĒżņ×ÉņÖĆ Ļ▓©ņÜĖĒżņ×ÉņäĖļīĆļź╝ ļ│┤ļéĖļŗż. ļ░░ļéśļ¼┤ ļČēņØĆļ│äļ¼┤ļŖ¼ļ│æņØś Ļ▓ĮņÜ░ ļ░░ļéśļ¼┤ņŚÉņä£ ļģ╣ļ│æĒżņ×ÉņÖĆ ļģ╣Ēżņ×ÉņäĖļīĆļź╝ ļ│┤ļé┤Ļ│Ā, Ē¢źļéśļ¼┤ņŚÉņä£ Ļ▓©ņÜĖĒżņ×ÉņäĖļīĆļź╝ ļ│┤ļé┤ļ®░, ņØ┤ ļģ╣ļ│æĻĘĀņØś Ļ▓ĮņÜ░ ņŚ¼ļ”äĒżņ×ÉļŖö ņĢäņ¦üĻ╣īņ¦Ć ļ░£Ļ▓¼ļÉśņ¦Ć ņĢŖņĢśļŗż(Lee ļō▒, 2017).
Ēśäņ×¼ ĻĄŁļé┤ņŚÉņä£ ļ│┤Ļ│ĀļÉ£ ļģ╣ļ│æĻĘĀņØĆ ņé░ņ┤łļéśļ¼┤ ļģ╣ļ│æĻĘĀ Coleosporium xanthoxyli, ĒĢ£ĻĄŁ ņ×öļöö zoysiagrass ļģ╣ļ│æĻĘĀ Puccinia zoysiae,Ļ░»ĻĖ░ļ”äļéśļ¼╝ ļģ╣ļ│æĻĘĀ Puccinia jogashimensis, ņ×ÉņŻ╝Ļ┤ŁņØ┤ļ░ź ļģ╣ļ│æĻĘĀ Puccinia oxalidis, ņ░Ėņåīļ”¼ņ¤üņØ┤ ļģ╣ļ│æĻĘĀ Puccinia phragmitisņØ┤ļ®░, ņØ┤ĒīØļéśļ¼┤ ļģ╣ļ│æĻĘĀĻ│╝ ĻĖ░ņŻ╝ņŗØļ¼╝ņØĆ ņĢäņ¦üĻ╣īņ¦Ć ļ│┤Ļ│ĀļÉśņ¢┤ ņ׳ņ¦Ć ņĢŖļŗż(Ko ļō▒, 2015; Lee ļō▒, 2004, 2018, 2020; Yoon ļō▒, 2013). ļö░ļØ╝ņä£ ņØ┤ĒīØļéśļ¼┤ ļģ╣ļ│æņØś ĒÜ©Ļ│╝ņĀüņØĖ ļ░®ņĀ£ņÖĆ Ļ▒┤Ļ░ĢĒĢ£ Ļ░ĆļĪ£ņłś ņ£Āņ¦Ćļź╝ ņ£äĒĢśņŚ¼ ņĀĢĒÖĢĒĢ£ ļ│æņøÉĻĘĀĻ│╝ ĻĖ░ņŻ╝ņŗØļ¼╝ņØś ĻĄ¼ļ¬ģņØ┤ ĒĢäņÜöĒĢ£ ņŗżņĀĢņØ┤ļŗż.
ļ│Ė ļģ╝ļ¼ĖņŚÉņä£ļŖö ņĀäļØ╝ļé©ļÅä Ļ░Ģņ¦äĻĄ░ ņä▒ņĀäļ®┤ ļ¼┤ņ£äņé¼ļĪ£ ņØ╝ļīĆ ņØ┤ĒīØļéśļ¼┤ Ļ░ĆļĪ£ņłśņŚÉņä£ ĒĢśņĀłĻĖ░ ļīĆļīĆņĀüņ£╝ļĪ£ ļ░£ņāØĒĢśļŖö ļģ╣ļ│æ ļ│æņøÉĻĘĀņØä ņŚ╝ĻĖ░ņä£ņŚ┤ ļČäņäØņØä ĒåĄĒĢśņŚ¼ ļÅÖņĀĢĒĢśņśĆĻ│Ā, Ļ┤Ćņ░░ļÉ£ ļģ╣ļ│æĻĘĀņŚÉ ļīĆĒĢ£ ĒśĢĒā£ņĀü ĒŖ╣ņ¦Ģ ļ░Å Ļ│äĒåĄĒĢÖņĀü ņ£ĀņŚ░Ļ┤ĆĻ│äļź╝ ļČäņäØĒĢśĻ│Ā, ņØ┤ĒīØļéśļ¼┤ ļģ╣ļ│æĻĘĀņØś ļÅÖņĀłĻĖ░ ņżæĻ░äĻĖ░ņŻ╝ņŗØļ¼╝ņØä ĒÖĢņØĖĒĢśņŚ¼ ļ│┤Ļ│ĀĒĢśĻ│Āņ×É ĒĢ£ļŗż. ļśÉĒĢ£ ļ│Ė ņŚ░ĻĄ¼ļź╝ ļ░öĒāĢņ£╝ļĪ£ ņØ┤ĒīØļéśļ¼┤ ļģ╣ļ│æņØś ĒÜ©Ļ│╝ņĀüņØĖ ļ░®ņĀ£ņŚ░ĻĄ¼ņŚÉ ĒÖ£ņÜ®ĒĢśĻ│Āņ×É ĒĢ£ļŗż.
ļ░£ļ│æĻ│╝ ļ│æņ¦Ģ. 2018ļģä 7ņøö ņĀäļØ╝ļé©ļÅä Ļ░Ģņ¦äĻĄ░ ņä▒ņĀäļ®┤ ļ¼┤ņ£äņé¼ļĪ£ņŚÉ ņŗØņ×¼ļÉ£ Ļ░ĆļĪ£ņłś ļ¬©ļōĀ ņØ┤ĒīØļéśļ¼┤ņØś ņ×Ä Ēæ£ļ®┤ņŚÉņä£ ĒÖ®ņāē ļ░śņĀÉņØ┤ ņŗ¼Ļ░üĒĢśĻ▓ī ļ░£ņāØĒĢśņśĆļŗż. ĒŖ╣Ē׳ ņ×Ä ņĢ×ļ®┤Ļ│╝ ņ×Äņ×ÉļŻ©ņŚÉņä£ ĒÖ®ņāē ļ░śņĀÉĻ│╝ ĒÖ®ņāē ļ░śņĀÉ ņżæņĢÖņŚÉ Ļ░łņāē ļ░śņĀÉņØ┤ Ļ┤Ćņ░░ļÉśņŚłĻ│Ā, ņ×Ä ļÆĘļ®┤ņŚÉņä£ļŖö ĒÖ®ņāē ļÅīĻĖ░ ļ¬©ņ¢æņØś ļģ╣Ēżņ×ÉĻĖ░(aecium)Ļ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 1A, B). ņØ┤ņÖĆ Ļ░ÖņØĆ ņ”ØņāüņØĆ ņŗ¼Ļ░üĒĢśĻ▓ī ļ»ĖĻ┤ĆņØä ĒĢ┤ņ│żņ£╝ļ®░, ņØ┤ĒīØļéśļ¼┤ņØś Ļ░ĆļĪ£ņłśļĪ£ņä£ņØś ņāüĒÆłņä▒ Ļ░Ćņ╣śņÖĆ Ļ▓ĮņĀ£ņä▒ņØä Ēü¼Ļ▓ī ļ¢©ņ¢┤ļ£©ļĀĖļŗż. ļ│æņøÉĻĘĀ ĒśĢĒā£ņĀü ĒŖ╣ņ¦ĢņØĆ Ļ┤æĒĢÖĒśäļ»ĖĻ▓Į(BX53, Olympus, Tokyo, Japan)ņØä ņØ┤ņÜ®ĒĢśņŚ¼ 400-1,000ļ░░ ļ░░ņ£©ļĪ£ Ļ┤Ćņ░░ĒĢśņśĆļŗż. ĻĘĖ Ļ▓░Ļ│╝, 28.84 ┬Ąm Ēü¼ĻĖ░ņØś ĻĄ¼ĒśĢņØś ĒĢśĒżņ×É(urediniospore)ņÖĆ 41.2 ┬Ąm Ēü¼ĻĖ░ņØś ĻĄ¼ĒśĢņØś ļģ╣Ēżņ×É(aeciospore)Ļ░Ć Ļ┤Ćņ░░ļÉśņŚłļŗż(Fig. 1C, D).
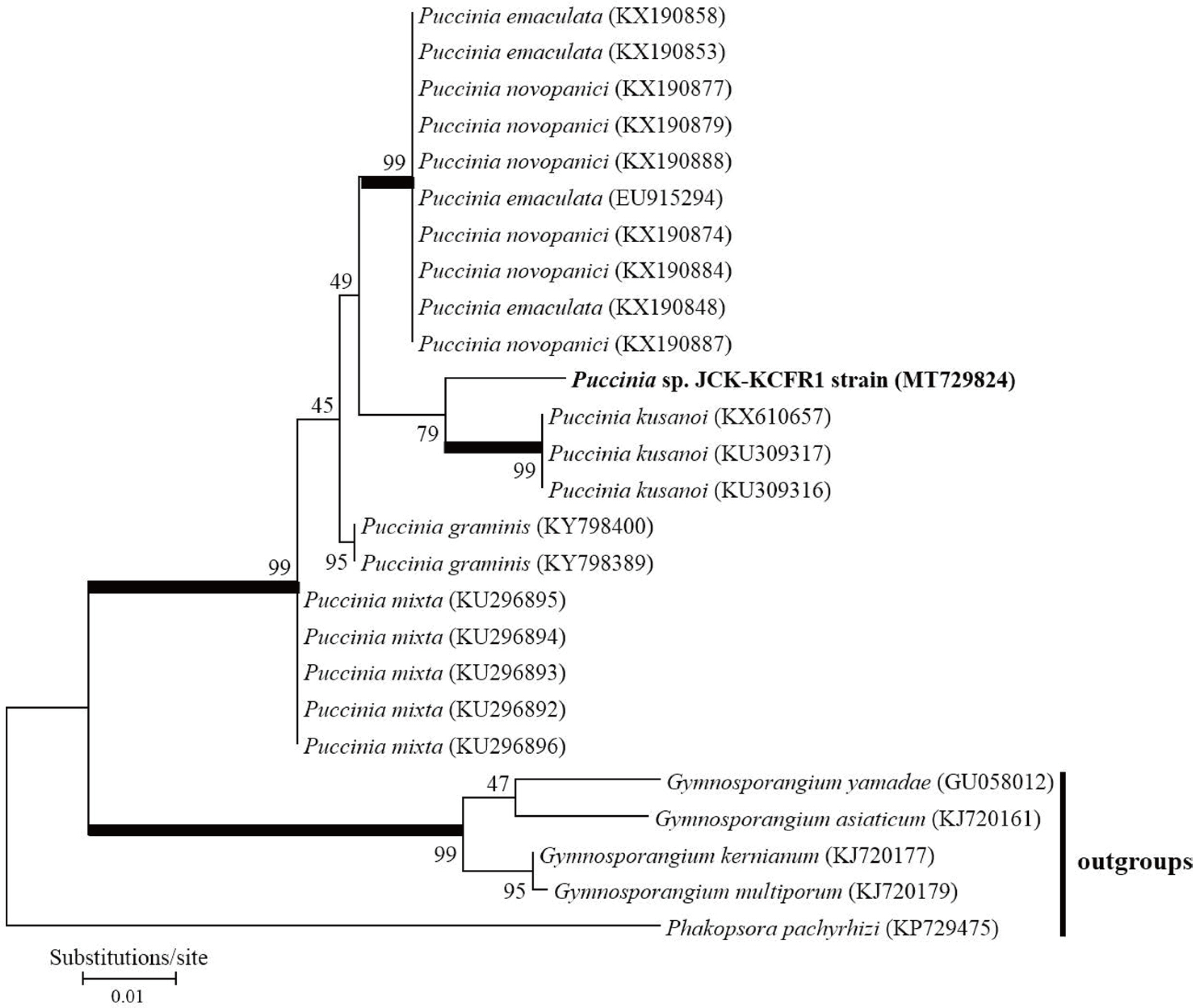
ļ│æņøÉĻĘĀņØś Ļ│äĒåĄĒĢÖņĀü ņ£ĀņŚ░Ļ┤ĆĻ│ä ļČäņäØ. Ļ┤Ćņ░░ļÉ£ ņØ┤ĒīØļéśļ¼┤ ļģ╣ļ│æĻĘĀņØś ļČäņ×ÉĻ│äĒåĄĒĢÖņĀü ņ£ĀņŚ░Ļ┤ĆĻ│äļź╝ ļČäņäØĒĢśĻĖ░ ņ£äĒĢśņŚ¼ ļ░£ļ│æĒżņןņŚÉņä£ ņ▒äņĘ©ĒĢ£ ņØ┤ĒīØļéśļ¼┤ ņ×Ä ļÆĘļ®┤ ļģ╣Ēżņ×ÉĻĖ░ņŚÉņä£ ļģ╣Ēżņ×Éļź╝ ņ▒äņ¦æĒĢśņśĆļŗż. ņ▒äņ¦æĒĢ£ ļģ╣Ēżņ×ÉņŚÉņä£ NucleoSpin Plant II kit (Macherey-Nagel, D├╝ren, Germany)ļź╝ ņØ┤ņÜ®ĒĢ£ ņČöņČ£ļ▓Ģņ£╝ļĪ£ genomic DNAļź╝ ņČöņČ£ĒĢśņśĆĻ│Ā, Beenken ļō▒(2012)ņØ┤ ļ│┤Ļ│ĀĒĢ£ small subunit rRNA, internal transcribed spacer, large subunit rRNA ļČĆņ£äļź╝ ņ”ØĒÅŁĒĢĀ ņłś ņ׳ļŖö ĒŖ╣ņØ┤ primer ņäĖĒŖĖ LRust1RņÖĆ LR6ļĪ£ PCRņØä ņłśĒ¢ēĒĢśņśĆļŗż. PCR Ēøä ņ”ØĒÅŁņé░ļ¼╝ņØä 1% agarose gelņŚÉņä£ ņĀäĻĖ░ņśüļÅÖĒĢśņŚ¼ bandļź╝ ĒÖĢņØĖĒĢ£ Ēøä, ņŚ╝ĻĖ░ņä£ņŚ┤ ļČäņäØņØä ņØśļó░ĒĢśņśĆļŗż(Genotech, Daejeon, Korea). PCR ņ”ØĒÅŁņé░ļ¼╝ņØś Ēü¼ĻĖ░ļŖö 726 bpļĪ£ ĒÖĢņØĖļÉśņŚłĻ│Ā, JCK-KCFR1ņØś ņŚ╝ĻĖ░ņä£ņŚ┤ņØä NCBI BLAST ņ¦äĒ¢ēĒĢ£ Ļ▓░Ļ│╝, Shen ļō▒(2017)ņØ┤ ļ│┤Ļ│ĀĒĢ£ ĒāĆņØ┤ņÖäņØś ņśźņé░ņŻĮ Yushan Cane (Yushania niitakayamensis)ņØś ļģ╣ļ│æĻĘĀ Puccinia kusanoi TNM F0029955 (KX610657)Ļ│╝ 97.53%ļĪ£ ņāüļÅÖņä▒ņØ┤ Ļ░Ćņן ļåÆņØĆ Ļ▓āņ£╝ļĪ£ ĒÖĢņØĖļÉśņŚłļŗż. ņØ┤ĒīØļéśļ¼┤ ļģ╣ļ│æĻĘĀņØś 726 bp ņŚ╝ĻĖ░ņä£ņŚ┤ņØĆ NCBI GenBankņŚÉ Puccinia sp. JCK-KCFR1 strain (MT729824)ņ£╝ļĪ£ ļō▒ļĪØĒĢśņśĆĻ│Ā, BLAST Ļ▓░Ļ│╝ļź╝ ĒåĄĒĢ┤ ņāüļÅÖņä▒ņØ┤ ņ׳ļŖö ņŚ╝ĻĖ░ņä£ņŚ┤ļōżņØä ņØ┤ņÜ®ĒĢśņŚ¼ MEGA 6.0 ĒöäļĪ£ĻĘĖļשņØś maximum parsimony ļČäņäØļ▓Ģņ£╝ļĪ£ maximum likelihood Ļ│äĒåĄļÅäļź╝ ĒåĄĒĢśņŚ¼ ĻĘ╝ņŚ░Ļ┤ĆĻ│äļź╝ ļČäņäØĒĢśņśĆļŗż(Dixon ļō▒, 2010; Tamura ļō▒, 2013). ĻĘĖ Ļ▓░Ļ│╝, P. kusanoiņóģĻ│╝ Ļ░Ćņן ĻĘ╝ņŚ░Ļ┤ĆĻ│äĻ░Ć Ļ░ĆĻ╣Øņ¦Ćļ¦ī ņāłļĪ£ņÜ┤ ņóģņØĖ Puccinia sp. JCK-KCFR1 strain (MT729824)ļĪ£ ĒÖĢņØĖļÉśņŚłļŗż(Fig. 2). FraitureņÖĆ Vanderweyen (2020)ņØś ļ│┤Ļ│ĀņŚÉ ņØśĒĢśļ®┤ P. kusanoiļŖö P. deutziae, comb. nov.ļĪ£ ņØ╝ļ│Ė, ĒāĆņØ┤ņÖä, ņśüĻĄŁ ļō▒ņŚÉņä£ ļīĆļéśļ¼┤Ļ░Ć ĻĖ░ņŻ╝ņŗØļ¼╝ņØĖ ļģ╣ļ│æĻĘĀņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņ¢┤ņĀĖ ņ׳ļŗż(HiratsukaņÖĆ Chen, 1991; Hiratsuka ļō▒, 1992; Reid, 1978; Shen ļō▒, 2017).
ņżæĻ░äĻĖ░ņŻ╝ ĒÖĢņØĖ. 2019ļģä 5ņøö ņĀäļØ╝ļé©ļÅä Ļ░Ģņ¦äĻĄ░ ņä▒ņĀäļ®┤ ļ¼┤ņ£äņé¼ļĪ£ņŚÉ ņŗØņ×¼ļÉ£ ņØ┤ĒīØļéśļ¼┤ ņŻ╝ļ│Ć ļīĆļéśļ¼┤ņØś ņ×Ä ņĢ×ļ®┤ņŚÉņä£ ļģ╣ļ│æ ļ│æņ¦ĢņØä Ļ┤Ćņ░░ĒĢśņśĆĻ│Ā, ņ×Ä ļÆĘļ®┤ņŚÉņä£ ņ¦ÖņØĆ Ļ░łņāēņ£╝ļĪ£ ļÅīņČ£ļÉśĻ│Ā ņé░ņ×¼ĒĢ£ ļÅÖĒżņ×ÉĒć┤(telium)ļź╝ Ļ┤Ćņ░░ĒĢśņśĆļŗż(Fig. 3A, B). ļ│æņøÉĻĘĀ ĒśĢĒā£ņĀü ĒŖ╣ņ¦ĢņØä Ļ┤æĒĢÖĒśäļ»ĖĻ▓Į(BX53, Olympus)ņ£╝ļĪ£ Ļ┤Ćņ░░ĒĢ£ Ļ▓░Ļ│╝, ņ×Ä ļÆĘļ®┤ņŚÉņä£ ļÅÖĒżņ×ÉĒć┤ņÖĆ ļÅÖĒżņ×É(teliospore)ļź╝ Ļ┤Ćņ░░ĒĢśņśĆļŗż(Fig. 3C). ļ░£ļ│æĒżņןņŚÉņä£ ņ▒äņĘ©ĒĢ£ ļīĆļéśļ¼┤ ņ×Ä ļÆĘļ®┤ ļÅÖĒżņ×ÉĒć┤ņŚÉņä£ ļÅÖĒżņ×Éļź╝ ņ▒äņ¦æĒĢśņŚ¼ ņØ┤ĒīØļéśļ¼┤ņØś ļģ╣ļ│æ ļ│æņøÉĻĘĀņØś ņŚ╝ĻĖ░ņä£ņŚ┤ ļČäņäØĻ│╝ Ļ░ÖņØĆ ļ░®ļ▓Ģņ£╝ļĪ£ genomic DNAļź╝ ņČöņČ£ĒĢśņśĆĻ│Ā, Ļ░ÖņØĆ primerļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņ”ØĒÅŁĒĢśņśĆļŗż. PCR Ēøä ļīĆļéśļ¼┤ ļÅÖĒżņ×ÉņØś ņ”ØĒÅŁņé░ļ¼╝Ļ│╝ 726 bpņØś ņØ┤ĒīØļéśļ¼┤ ļģ╣Ēżņ×ÉņØś ņ”ØĒÅŁņé░ļ¼╝ņØä ĒĢ©Ļ╗ś 1% agarose gelņŚÉņä£ ņĀäĻĖ░ņśüļÅÖĒĢ£ Ļ▓░Ļ│╝, ļæÉ ņ”ØĒÅŁņé░ļ¼╝ņØś DNA ņé¼ņØ┤ņ”łĻ░Ć ņØ╝ņ╣śĒĢśļŖö Ļ▓āņØä ĒÖĢņØĖĒĢśņśĆļŗż. ļīĆļéśļ¼┤ ļģ╣ļ│æ ļÅÖĒżņ×ÉņŚÉņä£ ņ¢╗ņØĆ PCR ņ”ØĒÅŁļÉ£ ņé░ļ¼╝ņØś ņŚ╝ĻĖ░ņä£ņŚ┤ ļČäņäØ ņŚŁņŗ£ ņØśļó░ĒĢśņśĆļŗż(Genotech). ĻĘĖ Ļ▓░Ļ│╝, ļīĆļéśļ¼┤ ļÅÖĒżņ×ÉņŚÉņä£ ņ¢╗ņØĆ ņŚ╝ĻĖ░ņä£ņŚ┤ņØ┤ ņØ┤ĒīØļéśļ¼┤ ļģ╣ļ│æĻĘĀņØś ņŚ╝ĻĖ░ņä£ņŚ┤ Puccinia sp. JCK-KCFR1 strain (MT729824)Ļ│╝ ņĀĢĒÖĢĒ׳ ņØ╝ņ╣śĒĢśļŖö Ļ▓āņØä ĒÖĢņØĖĒĢśņśĆļŗż.
ĻĄŁļé┤ņŚÉņä£ļŖö Ēśäņ×¼Ļ╣īņ¦Ć ņØ┤ĒīØļéśļ¼┤ņÖĆ ļīĆļéśļ¼┤ņŚÉņä£ ļģ╣ļ│æĻĘĀņØ┤ ļ│┤Ļ│ĀļÉ£ ļ░öĻ░Ć ņŚåņ£╝ļéś ļ│Ė ļģ╝ļ¼ĖņØä ĒåĄĒĢśņŚ¼ ņĀäļØ╝ļé©ļÅä Ļ░Ģņ¦äĻĄ░ ņä▒ņĀäļ®┤ ļ¼┤ņ£äņé¼ļĪ£ņŚÉ ņŗØņ×¼ļÉ£ ņØ┤ĒīØļéśļ¼┤ņÖĆ ņŻ╝ļ│Ć ļīĆļéśļ¼┤ņŚÉ ļ░£ņāØĒĢśļŖö ļģ╣ļ│æņØ┤ ļīĆļéśļ¼┤ ļģ╣ļ│æĻĘĀņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņ¢┤ņĀĖ ņ׳ļŖö P. kusanoiņÖĆ Ļ░Ćņן ĻĘ╝ņŚ░Ļ┤ĆĻ│äĻ░ĆĻ░ĆĻ╣īņÜ┤ ņāłļĪ£ņÜ┤ ņóģ Puccinia sp. JCK-KCFR1 strain (MT729824)ņŚÉ ņØśĒĢ┤ ļ░£ņāØĒĢśņśĆļŗżļŖö Ļ▓āņØä ĻĘ£ļ¬ģĒĢśņśĆļŗż. ļŹöļČłņ¢┤ ņØ┤ĒīØļéśļ¼┤ņÖĆ ļīĆļéśļ¼┤Ļ░Ć ĻĖ░ņŻ╝ĻĄÉļīĆĒĢśļ®┤ņä£ ļ│æĒÖśņØä ņÖäņä▒ĒĢśļŖö Ļ▓āņØä ņ▓śņØīņ£╝ļĪ£ ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļŗż.
2018ļģä 7ņøö ņĀäļØ╝ļé©ļÅä Ļ░Ģņ¦äĻĄ░ņØś Ļ░ĆļĪ£ņłś ņĀäņ▓┤ ņØ┤ĒīØļéśļ¼┤ņŚÉ ņŗ¼Ļ░üĒĢ£ ļģ╣ļ│æņ”ØņāüņØ┤ ļ░£Ļ▓¼ļÉśņ¢┤ ņ×ÄņØä ņ▒äņ¦æĒĢśņśĆļŗż. ņ▒äņ¦æĒĢ£ ņØ┤ĒīØļéśļ¼┤ ņ×Ä ņĢ×ļ®┤ņŚÉņä£ ĒÖ®ņāē ļ░Å Ļ░łņāēņØś ļ│æļ░śĻ│╝ ņ×Ä ļÆĘļ®┤ņŚÉņä£ ĒÖ®ņāēņØś ļģ╣Ēżņ×ÉĻĖ░
Ļ░ĆĻ┤Ćņ░░ļÉśņŚłĻ│Ā, Ēśäļ»ĖĻ▓ĮņĢäļלņŚÉņä£ 41.2 ┬Ąm Ēü¼ĻĖ░ņØś ĻĄ¼ĒśĢ ļģ╣Ēżņ×ÉņÖĆ28.84 ┬Ąm Ēü¼ĻĖ░ņØś ĻĄ¼ĒśĢ ĒĢśĒżņ×ÉĻ░Ć ĒÖĢņØĖļÉśņŚłļŗż. ņØ┤ĒīØļéśļ¼┤ ļģ╣ļ│æĻĘĀņØś ļČĆļČä small subunit rRNA, internal transcribed spacer (ITS) 1, 5.8S rRNA, ITS2, ļČĆļČä large subunit rRNA ņŚ╝ĻĖ░ņä£ņŚ┤ņØä ņØ┤ņÜ®ĒĢśņŚ¼ Ļ│äĒåĄĒĢÖņĀü ņ£ĀņŚ░Ļ┤ĆĻ│äļź╝ ļČäņäØĒĢ£ Ļ▓░Ļ│╝, ļīĆļéśļ¼┤ ļģ╣ļ│æĻĘĀņ£╝ļĪ£ ļ│┤Ļ│ĀļÉśņ¢┤ņĀĖ ņ׳ļŖö Puccinia kusanoiņÖĆ Ļ░ĆĻ╣īņÜ┤ ĻĘ╝ņŚ░Ļ┤ĆĻ│äļź╝ Ļ░Ćņ¦ĆĻ│Ā ņ׳ņŚłļŗż. ļśÉĒĢ£ 2019ļģä 5ņøö ļ¼┤ņ£äņé¼ļĪ£ ņØ┤ĒīØļéśļ¼┤ ņŻ╝ļ│ĆņŚÉ ņŗØņ×¼ļÉ£ ļīĆļéśļ¼┤ņŚÉņä£ļÅä ļģ╣ļ│æ ļ│æņ¦ĢņØ┤ Ļ┤Ćņ░░ļÉśņŚłĻ│Ā, ņ×Ä ļÆĘļ®┤ņŚÉņä£ ļÅÖĒżņ×ÉĒć┤ņÖĆ ļÅÖĒżņ×Éļź╝ ĒÖĢņØĖĒĢśņśĆņ£╝ļ®░, ļīĆļéśļ¼┤ņŚÉņä£ ņ▒äņ¦æĒĢ£ ļÅÖĒżņ×ÉņØś ņŚ╝ĻĖ░ņä£ņŚ┤ļČäņäØ Ļ▓░Ļ│╝, ņØ┤ĒīØļéśļ¼┤ ļģ╣ļ│æĻĘĀĻ│╝ 100% ņØ╝ņ╣śĒĢśņśĆļŗż. ļ│Ė ļģ╝ļ¼ĖņØĆ ļīĆļéśļ¼┤ ļģ╣ļ│æĻĘĀņ£╝ļĪ£ ņĢīļĀżņ¦ä P. kusanoiņÖĆ ĻĘ╝ņŚ░Ļ┤ĆĻ│äĻ░Ć Ļ░ĆĻ╣īņÜ┤ ņāłļĪ£ņÜ┤ ņóģ Puccinia sp. JCK-KCFR1 strain (MT729824)Ļ░Ć ĻĄŁļé┤ņŚÉņä£ ņØ┤ĒīØļéśļ¼┤ņÖĆ ļīĆļéśļ¼┤ļź╝ ĻĖ░ņŻ╝ĻĄÉļīĆĒĢśļ®░ ļģ╣ļ│æņØä ļ░£ņāØņŗ£ĒéżļŖö Ļ▓āņØä ņ▓śņØīņ£╝ļĪ£ ļ│┤Ļ│ĀĒĢ£ļŗż.
Acknowledgments
This research was supported by a grant from the National Institute of Biological Resources (NIBR), funded by the Ministry of Environment (MOE) of the South Korea (NIBR202018201).
Fig.┬Ā1
Rust disease caused by Puccinia sp. JCK-KCFR1 strain (MT729824) on fringe tree (Chionanthus retusus). (A) Symptoms of rust disease on leaves in July 2018. (B) Aecia of infected leaf back side. (C, D) Urediniospore and aeciospore by light microscope.

Fig.┬Ā2
Maximum likelihood phylogeny based on the small subunit rRNA, internal transcribed spacer, large subunit rRNA sequences. Branch support >45% from maximum parsimony bootstrap is indicated. The bootstrap consensus tree was inferred from 1,000 replicate and those above 90% indicated by bold lines. Bar=number of nucleotide substitutions per site.
References
Beenken, L. and Zoller, S. 2012. Rust fungi on Annonaceae II: the genus Dasyspora Berk. & M.A. Curtis. Mocologia 104: 659-681.

Dixon, L. J., Castlebury, L. A., Aime, M. C., Glynn, N. C. and Comstock, J. C. 2010. Phylogenetic relationships of sugarcane rust fungi. Mycol. Prog 9: 459-468.

Fraiture, A. and Vanderweyen, A. 2020. Species of Puccinia Pers. nom. sanct. (rust fungi) on Bambusoideae in Belgium and in Europe. Cryptogam. Mycol 41: 9-20.

Hiratsuka, N. and Chen, Z. C. 1991. A list of Uredinales collected from Taiwan. Trans. Mycol. Soc. Jpn 62: 3-22.
Hiratsuka, N., Sato, S., Katsuya, K., Kakishima, M., Hiratsuka, Y., Kaneko, S. et al. 1992. The Rust flora of Japan. Tsukuba Shuppankai Takezono, Ibaraki, Japan. pp. 1205 pp.
Ko, S.-J., Kim, H.-J., Myung, I.-S., Uhm, M.-J. and Choi, I.-Y. 2015. Occurrence of rust on Peucedanum japonicum caused by Puccinia jogashimensis in Korea. Res. Plant Dis 21: 337-340. (In Korean)

Korea Forest Service. 2019. Roadside trees and forests. Current status of street trees in Korea (based at the end of 2018). URL http://www.forest.go.kr/kfsweb/kfi/kfs/cms/cmsView.do?mn=NKFS_03_14_01_03_03&cmsId=FC_001302(In Korean)4 September 2020.
Lee, J. K., Cha, B., Shin, H. D. and Na, Y.-J. eds. by J. K. Lee, B. Cha, H. D. Shinand and Y.-J. Na, 2017. Tree diseases by biotic factors. In: Forest and Shade Tree Pathology, Hyangmunsa, Seoul, Korea. pp. 86-255. (In Korean)
Lee, S. K., Km, K. H., Lee, C. K., Kim, D. Y. and Hwang, J. H. 2004. Morphological features of Coleosporium xanthoxyli and its alternate host in Korea. Res. Plant Dis 10: 279-284. (In Korean)

Lee, S. H., Lee, C. K., Cho, S. E. and Shin, H. D. 2018. First report of rust caused by Puccinia oxalidis on Oxalis debilis var. corymbosa in Korea. Plant Dis 103: 148

Lee, S.-Y., Park, J.-W., Kang, I.-K. and Jung, H.-Y. 2020. First report of rust disease caused by Puccinia phragmitis on Rumex japonicus in Korea. . Res. Plant Dis 26: 53-56. (In Korean)

Shen, Y. M., Huang, T. C., Chung, W. H. and Hung, T. H. 2017. First report of rust caused by Puccinia kusanoi affecting Yushan cane (Yushania niitakayamensis) in Taiwan. Plant Dis 101: 385

- TOOLS
-
METRICS

- ORCID iDs
-
Jin-Cheol Kim

https://orcid.org/0000-0003-0753-1966 - Related articles
-
First Report of a Bracken Blight Disease Caused by Didymella sp.2019 September;25(3)




 PDF Links
PDF Links PubReader
PubReader Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print