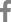|
 |
| Res. Plant Dis > Volume 26(1); 2020 > Article |
|
ņÜö ņĢĮ
2016ļģä ņĮ®ņØä ņ×¼ļ░░ĒĢśļŖö ĒżņןņŚÉņä£ ļ¦łļ”ä ņ”ØņāüņŚÉ ņØśĒĢ£ ņĮ®ņØś Ēö╝ĒĢ┤Ļ░Ć ņŗ¼ĒĢśĻ▓ī ļ░£ņāØĒĢśņśĆļŗż. ņ£Āļ¼śĻĖ░ ļĢīņŚÉļŖö ņלļĪØ ņ”ØņāüĻ│╝ ņ×ÉņŚĮņŚÉ Ļ░łņāē ļśÉļŖö Ļ▓ĆņØĆņāēņØś ļ░śņĀÉņØ┤ ļéśĒāĆļéśĻĖ░ ņŗ£ņ×æĒĢśļŗżĻ░Ć, 8ņøö ņØ┤Ēøä Ļ░£ĒÖöĻĖ░ņŚÉļŖö ņ¦ĆņāüļČĆ ņ×ÄņØ┤ ĒÖ®ĒÖöļÉśĻĖ░ ņŗ£ņ×æĒĢśļ®┤ņä£ ļČĆļČäņĀüņ£╝ļĪ£ Ļ░łļ│ĆļÉśņŚłļŗż. ņØ┤ ņŗ£ĻĖ░ņŚÉ ņ▒äņ¦æĒĢ£ ņĮ®ņØś ļ┐īļ”¼ļŖö ņāØņ£ĪņØ┤ ļ¦ÄņØ┤ ņ¢ĄņĀ£ļÉ£ ņāüĒā£ņØ┤ļ®░, Ēæ£Ēö╝ Ļ░Ć ļ▓ŚĻ▓©ņ¦Ćļ®┤ņä£ ĻĘĀĒĢĄņØ┤ ĒśĢņä▒ļÉśĻĖ░ ņŗ£ņ×æĒĢśņśĆļŗż. 9ņøö ņØ┤ĒøäļČĆĒä░ļŖö ņ¦ĆņāüļČĆņØś ļ¦łļ”ä ņ”ØņāüņØ┤ ļŹö ļÜ£ļĀĘĒĢ┤ņĪīņ£╝ļ®░ Ļ│Āņé¼ĒĢśĻĖ░ ņŗ£ņ×æĒĢśņśĆĻ│Ā, ņłśņ╣©ņāü ļ│æņ¦ĢņØä ļ│┤ņØ┤ļŹś ņżäĻĖ░ņŚÉļÅä ĻĘĀĒĢĄņØ┤ ĒśĢņä▒ļÉśņŚłļŗż. ņłśĒÖĢĻĖ░ņØĖ 10 ņøö ņżæņł£ ņØ┤ĒøäņŚÉļŖö ņżäĻĖ░ņØś Ēæ£Ēö╝Ļ░Ć ļ▓ŚĻ▓©ņ¦Ćļ®┤ņä£ Ēö╝ņĖĄ ļČĆņ£äņŚÉ ņåīļ”ĮĻĘĀ ĒĢĄņØ┤ ļŗżļ¤ēņ£╝ļĪ£ ĒśĢņä▒ļÉśņŚłļŗż. ņØ┤ļ¤░ ļ│æņ¦Ģņ£╝ļĪ£ļČĆĒä░ ļČäļ”¼ĒĢ£ ļ│æņøÉĻĘĀņØĆ 32-35┬░CņŚÉņä£ ĻĘĀņé¼ ņāØņ£ĪņØ┤ Ļ░Ćņן ņ¢æĒśĖĒĢśņśĆĻ│Ā, ņåīļ”ĮĻĘĀĒĢĄņØś ĒśĢņä▒ņØĆ 20-28┬░CņŚÉņä£ Ļ░Ćņן ļ¦ÄņĢśļŗż. ļ│æņøÉĻĘĀņØś ĻĘĀĒĢÖņĀüņØĖ ĒśĢĒā£ Ļ┤Ćņ░░Ļ│╝ internal transcribed spacer ņśüņŚŁ ņ£ĀņĀäņ×ÉņØś ņŚ╝ĻĖ░ņä£ņŚ┤ ļČäņäØņØä ņŗżņŗ£ĒĢ£ Ļ▓░Ļ│╝, ļ│æņøÉĻĘĀņØĆ Macrophomina phaseolinaļĪ£ ļÅÖņĀĢļÉśņŚłļŗż. ļśÉĒĢ£ ņØ┤ņæżņŗ£Ļ░£ļź╝ ņØ┤ņÜ®ĒĢ£ ņØĖĻ│ĄņĀæņóģņŚÉņä£ļÅäĒżņןņŚÉņä£ņÖĆ Ļ░ÖņØĆ ļ│æņ¦ĢņØä ļ│┤ņśĆņØä ļ┐Éļ¦ī ņĢäļŗłļØ╝, ņ×¼ļČäļ”¼ņŚÉņä£ļÅä ļÅÖņØ╝ĒĢ£ ļ│æņøÉĻĘĀņØ┤ ļČäļ”¼ŃåŹļÅÖņĀĢļÉśņŚłļŗż. ĻĘĖ Ļ▓░Ļ│╝ ņØ┤ ļ│æņØä ņĮ® ĻĘĀĒĢĄļ¦łļ”äļ│æ(Ļ░Ćņ╣Ł)ņ£╝ļĪ£ ļ│┤Ļ│ĀĒĢśļŖö ļ░öņØ┤ļŗż.
ABSTRACT
Stem blight symptom of soybean was severely developed in 2016 in Hwaseong and Yeoncheon. During the seedling period, the damping-off of seedlings and the brown or black spots of cotyledons were observed. After August, the leaves began to be yellowed, and partially browned areas on leaves began to develop. After September, microsclerotia began to form even on the surface of the stems that had exhibited water-soaking symptom. After mid-October of the harvest season, the epidermis of the stem was peeled off, resulting in the formation of a large number of microsclerotia in the cortex. The pathogens isolated from these symptoms were the best in mycelial growth at 32-35┬░C, and the formation of microsclerotia was the most at 20-28┬░C. The pathogen was identified as Macrophomina phaseolina through the morphological characteristics of the pathogen and the sequencing of the internal transcribed spacer region gene. In addition, when inoculated with a soybean stem using toothpicks cultured with the pathogen, the same symptoms as seen on the soybean field occurred. When the pathogen was re-isolated at the lesion site, the same pathogen was isolated and identified as Macrophomina phaseolina. Based on the results, the disease is reported as soybean charcoal rot.
ņĮ®(Glycine max Merr.)ņØĆ ļÉ£ņן, Ļ░äņן ļō▒ ņĀäĒåĄņØīņŗØņØś ņøÉļŻīļ┐Éļ¦ī ņĢäļŗłļØ╝, ļŗżņ¢æĒĢ£ ņāØļ”¼ņĀü ĒÜ©Ļ│╝ļź╝ Ļ░Ćņ¦ĆĻ│Ā ņ׳ĻĖ░ ļĢīļ¼ĖņŚÉ ņØśņĢĮ, ņé¼ļŻī, Ļ│ĄņŚģņÜ®Ļ│╝ ņä¼ņ£Ā ļō▒ņØś ņøÉļŻīļĪ£ Ļ┤æļ▓öņ£äĒĢśĻ▓ī ņé¼ņÜ®ļÉśĻ│Ā ņ׳ņ¦Ćļ¦ī, ĻĄŁļé┤ ņĮ® ņ×¼ļ░░ļ®┤ņĀüĻ│╝ ņāØņé░ļ¤ēņØĆ Ļ│äņåŹ Ļ░ÉņåīĒĢśĻ│Ā ņ׳ļŗż. 1981ļģäņŚÉ 201,722haņŚÉņä£ 256,851ĒåżņØ┤ ņāØņé░ļÉśļŗżĻ░Ć, 2000ļģä ļōżņ¢┤ņśżļ®┤ņä£ ņ×¼ļ░░ ļ®┤ ņĀüņØĆ 86,176 haļĪ£, ņāØņé░ļ¤ēņØĆ 113,196Ēåżņ£╝ļĪ£ Ļ░ÉņåīĒĢśņśĆļŗż(Korea Statistical Information Service, 2020). Ļ░Éņåī ņČöņäĖļŖö Ļ│äņåŹļÉśņ¢┤ 2018ļģäņØś ņĮ® ņ×¼ļ░░ļ®┤ņĀüĻ│╝ ņāØņé░ļ¤ēņØĆ 50,638 haņÖĆ 89,410ĒåżĻ╣īņ¦Ć ĒĢśļØĮĒĢśņśĆļŗż. ņØ┤ņ▓śļ¤╝ ņĮ®ņØĆ ņ×¼ļ░░ļ®┤ņĀüĻ│╝ ņāØņé░ļ¤ēņØ┤ Ļ░ÉņåīĒĢśĻ│Ā ņ׳ņØä ļ┐Éļ¦ī ņĢäļŗłļØ╝, ņ×¼ļ░░ ĻĖ░Ļ░ä ņżæņŚÉļŖö ņŚ¼ļ¤¼ Ļ░Ćņ¦Ć ņŗØļ¼╝ļ│æņøÉņ▓┤Ļ░Ć ņ╣©ņ×ģĒĢśņŚ¼ ļŗżņ¢æĒĢ£ ļ│æņØ┤ ļ░£ņāØĒĢśļ®░ ņāØņé░ļ¤ēņØ┤ ņ£äĒśæļŗ╣ĒĢśĻ│Ā ņ׳ļŗż. ņĀä ņäĖĻ│ä ņĀüņ£╝ļĪ£ ņĮ®ņØś ņāØņé░ļ¤ēņØä ļ¢©ņ¢┤ļ£©ļ”¼ļŖö ņżæņÜöĒĢ£ ļ│æņ£╝ļĪ£ļŖö ņŗ£ņŖżĒŖĖņäĀņČ®ļ│æ, Rhizoctonia, Pythium ļō▒ņŚÉ ņØśĒĢ£ ņ£Āļ¼śĻĖ░ņØś ļ│æ, MacrophominaņŚÉ ņØśĒĢ£ charcoal rot, FusariumņŚÉ ņØśĒĢ£ sudden death syndrome, SeptoriaņŚÉ ņØśĒĢ£ Ļ░łņāēļ¼┤ļŖ¼ļ│æ ļō▒ņØ┤ ļ│┤Ļ│ĀļÉśņ¢┤ ņ׳ļŗż (Allen ļō▒, 2017). ĻĄŁļé┤ņŚÉļŖö ņ¦äĻĘĀņØ┤ ņØ╝ņ£╝ĒéżļŖö ļ│æņØ┤ ĒāäņĀĆļ│æņØä ļ╣äļĪ» ĒĢśņŚ¼ 24ņóģ, ņäĖĻĘĀņØ┤ ņØ╝ņ£╝ĒéżļŖö ļ│æņØ┤ ļČłļ¦łļ”äļ│æ ļō▒ 4ņóģ, ļ░öņØ┤ļ¤¼ņŖżņŚÉ ņØśĒĢ£ ļ│æĻ│╝ ņäĀņČ®ņŚÉ ņØśĒĢ£ ļ│æņØ┤ Ļ░üĻ░ü 4ņóģĻ│╝ 3ņóģņö®ņØ┤ ļ│┤Ļ│ĀļÉśņ¢┤ ņ׳ ļŗż(Korean Society of Plant Pathology, 2009).
ĻĄŁņĀ£ņĀüņ£╝ļĪ£ļÅä ņĮ®ņØś ņŻ╝ņÜöĒĢ£ ņāØņé░ņ¦ĆņØĖ ļ»ĖĻĄŁĻ│╝ ņ║Éļéśļŗż ņś©ĒāĆļ”¼ņśż ņ¦ĆņŚŁņØś 2010ļģäļČĆĒä░ 2014ļģäĻ╣īņ¦Ć 5ļģäĻ░äņØś ļłäņĀü ņāØņé░ļ¤ēņØĆ 172ņ¢Ą ļČĆņģĖņØĖļŹ░, ļÅÖņØ╝ĒĢ£ ĻĖ░Ļ░ä ļÅÖņĢł ļ│æņ£╝ļĪ£ ņØĖĒĢ£ ņĮ® ņāØņé░ļ¤ē Ļ░ÉņåīļŖö ņĀäņ▓┤ ņāØņé░ļ¤ēņØś 12.5%ņŚÉ ĒĢ┤ļŗ╣ĒĢśļŖö 21ņ¢Ą ļČĆņģĖņŚÉ ļŗ¼ĒĢ£ļŗż(Allen ļō▒, 2017). ļ░£ņāØĒĢśļŖö ņŻ╝ņÜö ļ│æņØĆ ņ¦ĆņŚŁņŚÉ ļö░ļØ╝ņä£ ņ░©ņØ┤Ļ░Ć ņ׳ļŖöļŹ░, ļ»ĖĻĄŁ ļČüļČĆ ņ¦ĆņŚŁņØĆ ņĮ® ņŗ£ņŖżĒŖĖņäĀņČ®ņŚÉ ņØśĒĢ£ Ēö╝ĒĢ┤Ļ░Ć Ļ░Ćņן ņ╗ĖļŹś ļ░śļ®┤ņŚÉ, ļé©ļČĆ ņ¦ĆņŚŁņŚÉņä£ļŖö 2010ļģäļČĆĒä░ 2012ļģäĻ╣īņ¦Ć ņŚ░ 3ļģäĻ░ä charcoal rotņŚÉ ņØśĒĢ£ Ēö╝ĒĢ┤Ļ░Ć Ļ░Ćņן ņ╗Ėļŗż. ļ»ĖĻĄŁ ļé©ļČĆ ņ¦ĆņŚŁņŚÉņä£ ņĮ® ņāØņé░ļ¤ē Ļ░ÉņåīņØś ņŻ╝ļÉ£ ņøÉņØĖņØ┤ ļÉśļŖö charcoalrotņØĆ MacrophominaĻ░Ć ņØ╝ņ£╝ĒéżļŖö ļ│æņ£╝ļĪ£, Ļ│Āņś© Ļ▒┤ņĪ░ĒĢ£ ņ¦ĆņŚŁņŚÉņä£ ļ░£ņāØņØ┤ ņŗ¼ĒĢśļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ļŗż. ĻĘĖļ¤░ļŹ░ ņĄ£ĻĘ╝ ņĮ® ņ×¼ļ░░ ĻĖ░Ļ░ä ļÅÖņĢłņØś ĻĄŁļé┤ ĻĖ░ņāü ņāüĒÖ®ņØ┤ Ļ│Āņś©Ļ▒┤ ņĪ░ĒĢ┤ņ¦ĆļŖö Ļ▓ĮĒ¢źņØä ļ│┤ņØ┤Ļ│Ā ņ׳ņ¢┤, ĒżņןņŚÉņä£ ņŻ╝ņÜö ļ│æņØś ļ░£ņāØņØ┤ ļ│ĆĒÖöĒĢĀ ņłś ņ׳ļŗżļŖö ņÜ░ļĀżļź╝ ļé│Ļ│Ā ņ׳ļŗż. 1980ļģäņŚÉ 11.2┬░CņØ┤ņŚłļŹś ņŚ░ĒÅē ĻĘĀ ĻĖ░ņś©ņØ┤ 2019ļģäņŚÉļŖö 13.5┬░CļĪ£ ņāüņŖ╣ĒĢśņśĆņ£╝ļ®░, ņĮ® ņ×¼ļ░░ ĻĖ░Ļ░äņØĖ 5ņøöļČĆĒä░ 10ņøöĻ╣īņ¦Ć 6Ļ░£ņøöĻ░äņØś ĒÅēĻĘĀ Ļ░Ģņłśļ¤ēņØä ļ│┤ņĢäļÅä 2013ļģäļČĆĒä░ 2017ļģäĻ╣īņ¦Ć 5ļģäĻ░äņØĆ Ļ│äņåŹ 150 mm ņØ┤ĒĢśļź╝ ĻĖ░ļĪØĒĢśĻ│Ā ņ׳ļŗż (Korea Meteorological Administration, 2020).
ĻĖ░ņāüņØ┤ Ļ│Āņś© Ļ▒┤ņĪ░ĒĢ┤ņ¦Ćļ®┤ņä£ 2016ļģäņŚÉ Ļ▓ĮĻĖ░ļÅä ĒÖöņä▒Ļ│╝ ņŚ░ņ▓£ņ¦ĆņŚŁņØś ĒżņןņŚÉņä£ ņ×¼ļ░░ĒĢśļŹś ņĮ®ņØ┤ ņŗ¼ĒĢśĻ▓ī ņŗ£ļō£ļŖö ņ”ØņāüņØ┤ ļéśĒāĆļé¼ļŗż. ĻĄŁ ļé┤ņŚÉņä£ ņĮ® ļ¦łļ”ä ņ”ØņāüņØä ņØ╝ņ£╝Ēé©ļŗżĻ│Ā ļ│┤Ļ│ĀļÉ£ ļ│æņ£╝ļĪ£ļŖö Diaporthe ņŚÉ ņØśĒĢ£ ļ»ĖņØ┤ļØ╝ļ│æ, FusariumņŚÉ ņØśĒĢ£ ņŗ£ļōżņØīļ│æ, SclerotiumņŚÉ ņØśĒĢ£ ĒØ░ļ╣äļŗ©ļ│æ ļō▒ņØ┤ ņ׳ņ¦Ćļ¦ī(Korean Society of Plant Pathology, 2009), ņĀä ņäĖĻ│ä ņĮ® ņŻ╝ņÜö ņāØņé░ 10Ļ░£ĻĄŁņØś ņāØņé░ļ¤ē Ļ░ÉņåīņØś ņøÉņØĖ ņżæ ļäż ļ▓łņ¦ĖļĪ£ ĒÅēĻ░ĆļÉĀ ļ¦īĒü╝ Ēü░ Ēö╝ĒĢ┤ļź╝ ņŻ╝ļŖö Macrophomina phaseolinaņŚÉ ņØśĒĢ£ charcoal rotņØĆ ņĢīļĀżņĀĖ ņ׳ņ¦Ć ņĢŖņØĆ ņāüĒā£ņØ┤ļŗż (Wrather ļō▒, 1997). ņØ┤ ļ│æņØĆ ļ│æņøÉĻĘĀņØ┤ ņĮ® ļ┐īļ”¼ļź╝ ņ╣©ņ×ģĒĢ£ Ēøä, ņäĖ ĒżĻ░äĻĘ╣ņØä ĒåĄĒĢ┤ņä£ ņ£ĀĻ┤ĆņåŹ ļČĆņ£äņØś ļ¼╝Ļ┤ĆĻ╣īņ¦Ć ņØ┤ļÅÖĒĢśņŚ¼ ņ£ĀĻ┤ĆņåŹ ņĪ░ņ¦üņØä ĻĖ░Ļ│äņĀüņ£╝ļĪ£ ĒÅÉņćäņŗ£ņ╝£ ņŗ£ļōżņØīĻ│╝ ļ¦łļ”ä ņ”ØņāüņØ┤ ļ░£ņāØĒĢśļŖö ļ│æņØ┤ļŗż(SmithņÖĆ Wyllie, 1999). ļ░£ļ│æ ĒøäĻĖ░Ļ░Ć ļÉśļ®┤ ņØ┤ ļ│æņØś ĒŖ╣ņ¦ĢņĀüņØĖ Ēæ£ņ¦ĢņØĖ ņåīļ”ĮĻĘĀĒĢĄ(microsclerotia)ņØ┤ ļ┐īļ”¼ņÖĆ ņżäĻĖ░ņĪ░ņ¦üņŚÉ ļŗżļ¤ē ĒśĢņä▒ļÉ£ļŗż(Gupta ļō▒, 2012). ņØ┤ ļ│æņøÉĻĘĀņŚÉ Ļ░ÉņŚ╝ļÉ£ ĻĖ░ņŻ╝ļŖö ņ┤łĻĖ░ņŚÉļŖö ļÜ£ļĀĘĒĢ£ ņ”ØņāüņØä ļéśĒāĆļé┤ņ¦Ć ņĢŖņ¦Ćļ¦ī, Ļ│Āņś©Ļ▒┤ņĪ░ĒĢ£ ĒÖśĻ▓ĮņĪ░Ļ▒┤ņØ┤ ņ¦ĆņåŹļÉĀ Ļ▓ĮņÜ░ ņŗ£ļōżņØī ņ”ØņāüĻ│╝ Ļ┤┤ņé¼ņ”ØņāüņØ┤ ņ┤ēņ¦äļÉśļŖö Ļ▓āņ£╝ļĪ£ ņĢīļĀżņĀĖ ņ׳ļŗż(Twizeyimana ļō▒, 2012).
ļ│Ė ņŚ░ĻĄ¼ļŖö 2016ļģä Ļ│Āņś©Ļ▒┤ņĪ░ĒĢ£ ĻĖ░ņāü ņĪ░Ļ▒┤ņŚÉņä£ ņŗ£ļōżņØī ņ”ØņāüņØä ļ│┤ņØĖ ņĮ®ņØä Ļ▓ĮĻĖ░ļÅä ĒÖöņä▒Ļ│╝ ņŚ░ņ▓£ņØś ņĮ® ņ×¼ļ░░ ĒżņןņŚÉņä£ ņ▒äņ¦æĒĢśņŚ¼,ņŗ£ļōżņØī ņ”ØņāüņØś ņøÉņØĖņØ┤ ļÉśļŖö ļ│æņøÉĻĘĀņØä ļČäļ”¼ĒĢśņŚ¼ ņ£ĀņĀäņ×É ņłśņżĆņŚÉņä£ ļÅÖņĀĢĒĢśĻ│Ā, ĻĘĀĒĢÖņĀü ĒŖ╣ņ¦ĢĻ│╝ ļ│æņøÉņä▒ ļō▒ņØä ņĪ░ņé¼ĒĢśņŚ¼ ļ│┤Ļ│ĀĒĢśĻ│Āņ×ÉĒĢ£ļŗż.
2016ļģä 7ņøöļČĆĒä░ 10ņøöĻ╣īņ¦Ć Ļ▓ĮĻĖ░ļÅä ĒÖöņä▒Ļ│╝ ņŚ░ņ▓£ņ¦ĆņŚŁņŚÉņä£ ņŗ£ļōżņØī ņ”ØņāüņØä ļ│┤ņØ┤ļŖö ņĮ®ņØä ņ▒äņ¦æĒĢśņśĆļŗż. ņłśņ¦æĒĢ£ ļ│æļōĀ ņĮ®ņŚÉņä£ ļ│æņøÉĻĘĀņØä ļČäļ”¼ĒĢśĻĖ░ ņ£äĒĢśņŚ¼ Ļ░ÉņŚ╝ļÉ£ ņĪ░ņ¦üņØä ņלļØ╝ 1%ņ░©ņĢäņŚ╝ņåīņé░ļéśĒŖĖļź©(NaOCl) ņÜ®ņĢĪņ£╝ļĪ£ 1ļČäĻ░ä Ēæ£ļ®┤ ņé┤ĻĘĀĒĢśĻ│Ā ņé┤ĻĘĀņłśļĪ£ 3ĒÜī ņäĖņ▓ÖĒĢśņśĆļŗż. ļ®ĖĻĘĀļÉ£ ņŚ¼Ļ│╝ņ¦ĆņŚÉņä£ ļ¼╝ĻĖ░ļź╝ ņĀ£Ļ▒░ĒĢ£ ļŗżņØī, potato dextrose agar (PDA, Difco, Detroit, MI, USA) ļ░░ņ¦Ćņ£äņŚÉ ņś¼ļĀżļåōĻ│Ā 28┬░CņŚÉņä£ 3ņØ╝Ļ░ä ļ░░ņ¢æĒĢśņśĆļŗż. ļ│æļōĀ ņĪ░ņ¦üņŚÉņä£ ņ×ÉļØ╝ļéśņś© ĻĘĀņé¼ņØś ņäĀļŗ©ļČĆņŚÉņä£ ĻĘĀņé¼ ņĪ░Ļ░üņØä ļ¢╝ņ¢┤ PDA ņé¼ļ®┤ļ░░ņ¦ĆņŚÉ ņĀæņóģĒĢ£ Ēøä 4┬░CņŚÉņä£ ļ│┤Ļ┤ĆĒĢśļ®░ ņŗżĒŚśņŚÉ ņé¼ņÜ®ĒĢśņśĆļŗż. ļśÉĒĢ£ ņĮ® ņØ┤ņÖĖņØśņ×æļ¼╝ ņżæņŚÉņä£ ņ░ĖĻ╣©, Ēīź, ļģ╣ļæÉ, ļĢģņĮ® ļō▒ņŚÉņä£ ņŗ£ļōżņØī ņ”ØņāüņØä ļ│┤ņØ┤ļŖöĻ░£ņ▓┤ļź╝ ņ▒äņ¦æĒĢśĻ│Ā ļČäļ”¼ļÉśļŖö ļ│æņøÉĻĘĀņØä ĒśĢĒā£ņĀüņ£╝ļĪ£ ļÅÖņĀĢĒĢśņśĆļŗż.
ļ│æņøÉĻĘĀ ļ░░ņ¢æņŚÉ ņĀüĒĢ®ĒĢ£ ļ░░ņ¦Ćļź╝ ņĪ░ņé¼ĒĢśĻĖ░ ņ£äĒĢ┤ņä£ ļČäļ”¼ĒĢ£ M. phaseolina HSW16-141 ĻĘĀņŻ╝ļź╝ 28┬░CņØś PDA ļ░░ņ¦ĆņŚÉņä£ 3ņØ╝Ļ░ä ļ░░ņ¢æĒĢ£ Ēøä, ĻĘĀņé¼ ņäĀļŗ©ļČĆņŚÉņä£ ņ¦üĻ▓Į 7 mmņØś ĻĘĀņé¼ ņĪ░Ļ░üņØä ļ¢╝ņ¢┤ļé┤ņ¢┤ ņāłļĪ£ņÜ┤ PDA ļ░░ņ¦ĆņŚÉ ņĀæņóģĒĢśĻ│Ā, ņĀĢĒĢ┤ņ¦ä ņś©ļÅä(20┬░C, 25┬░C, 30┬░C, 32┬░C, 35┬░C, 37┬░C, 40┬░C)ņŚÉņä£ ļ░░ņ¢æĒĢśļ®░ ĻĘĀņ┤ØņØś ņ¦üĻ▓ĮņØä ņĪ░ņé¼ĒĢśņśĆļŗż.
ChidambaramĻ│╝ Mathur (1975)ņØś ļ░®ļ▓ĢņŚÉ ļö░ļØ╝ ļČäņāØĒżņ×Éļź╝ ĒśĢņä▒ņŗ£ņ╝░ļŗż. ļ│┤ļ”¼ ņ×ÄņØä ņĀüļŗ╣ĒĢ£ Ēü¼ĻĖ░ļĪ£ ņ×ÉļźĖ Ēøä ĒØÉļź┤ļŖö ļ¼╝ņŚÉ ņäĖņ▓ÖĒĢśņŚ¼ Ļ▒┤ņĪ░ņŗ£Ēé© Ēøä, 121┬░CņŚÉņä£ 15ļČäĻ░ä ļ®ĖĻĘĀĒĢśņśĆļŗż. ļ®ĖĻĘĀĒĢ£ ļ│┤ļ”¼ ņ×ÄņØĆ ļ»Ėļ”¼ ņżĆļ╣äĒĢ┤ ļæö 1.5% ļ¼╝ĒĢ£ņ▓£ļ░░ņ¦ĆņŚÉ ņś¼ļ”░ Ēøä, PDA ļ░░ņ¦ĆņŚÉņä£ 48ņŗ£Ļ░ä ļ░░ņ¢æĒĢ£ ļ│æņøÉĻĘĀ ĻĘĀņ┤Ø ņäĀļŗ©ņŚÉņä£ ĻĘĀņé¼ ņĪ░Ļ░üņØä ļ¢╝ņ¢┤ ņĀæņóģĒĢśņśĆļŗż. ļ│æņøÉĻĘĀņØä ņĀæņóģĒĢ£ ļ│┤ļ”¼ ņ×ÄņØĆ 30┬░CņŚÉņä£ 12ņŗ£Ļ░äņö® Ļ┤æ/ņĢö ņĪ░Ļ▒┤ņØä ņ£Āņ¦ĆĒĢśļ®░ 7ņØ╝Ļ░ä ļ│┤Ļ┤ĆĒĢśĻ│Ā,ņ×Ä ņ£äņŚÉ ĒśĢņä▒ļÉ£ ļČäņāØĒżņ×ÉĻ░üĻ│╝ ļČäņāØĒżņ×É ĻĘĖļ”¼Ļ│Ā ņåīļ”ĮĻĘĀĒĢĄ ļō▒ņØäĻ┤Ćņ░░ĒĢśņśĆļŗż.
ļ│æņøÉĻĘĀņØś ļ│æņøÉņä▒ Ļ▓ĆņĀĢņØĆ Gopala ļō▒(2016)ņØśņŗżĒŚś ļ░®ļ▓ĢņØä Ļ░£ņäĀĒĢśņŚ¼ ņŗżņŗ£ĒĢśņśĆļŗż. M. phaseolina HSW16-141 ĻĘĀņŻ╝ļź╝ 32┬░CņØś PDA ļ░░ņ¦Ć(ņĢöņĪ░Ļ▒┤)ņŚÉņä£ 3ņØ╝Ļ░ä ļ░░ņ¢æĒĢśņśĆļŗż. ņØ┤ņæż ņŗ£Ļ░£ļź╝ 12 mm (ĻĖĖņØ┤)ļĪ£ ņ×ÉļźĖ Ēøä 121┬░CņŚÉņä£ 30ļČä ļÅÖņĢł 1ņØ╝ Ļ░äĻ▓® ņ£╝ļĪ£ ņ┤Ø 2ĒÜī ļ®ĖĻĘĀĒĢśņśĆļŗż. ņāłļĪŁĻ▓ī ņżĆļ╣äĒĢ£ PDA ļ░░ņ¦Ć(300 ┬Ąg/mlņØś streptomycinņØä ņ▓©Ļ░Ć)ņŚÉ ļ®ĖĻĘĀĒĢ£ ņØ┤ņæżņŗ£Ļ░£ 5Ļ░£ļź╝ ņś¼ļĀżļåōņØĆ ļŗżņØī, M. phaseolina HSW16-141ņØś ĻĘĀņ┤Ø ņäĀļŗ©ņŚÉņä£ ņ¦üĻ▓Į 7 mmņØśĻĘĀņé¼ ņĪ░Ļ░üņØä ņלļØ╝ļé┤ņ¢┤ ĒĢśļéśņØś ĒÄśĒŖĖļ”¼ ņĀæņŗ£ļŗ╣ 7Ļ░£ņö® ņĀæņóģĒĢśņśĆļŗż. ļ│æņøÉĻĘĀņØĆ 32┬░C ņĢöņĪ░Ļ▒┤ņŚÉņä£ 7ņØ╝Ļ░ä ļ░░ņ¢æĒĢśņŚ¼, ņĀæņóģņøÉņ£╝ļĪ£ ņé¼ņÜ®ĒĢśņśĆņ£╝ļ®░, ļīĆņøÉņĮ®ņØä ņś©ņŗżņŚÉņä£ ņ×¼ļ░░ĒĢśņŚ¼ ļ│æņøÉņä▒ ņŗżĒŚśņŚÉ ņé¼ņÜ® ĒĢśņśĆļŗż. ņ×¼ļ░░ņŚÉ ņé¼ņÜ®ĒĢ£ ņøÉņśłņÜ® ņāüĒåĀļŖö 121┬░CņŚÉņä£ 60ļČäĻ░ä 1ņØ╝ Ļ░äĻ▓®ņ£╝ļĪ£ ņ┤Ø 2ĒÜī ļ®ĖĻĘĀĒĢ£ Ēøä ĒżĒŖĖ(ņ¦üĻ▓Į, 10 cm; ļåÆņØ┤, 9 cm)ņŚÉ ļŗ┤Ļ│Ā, 2% NaOClņŚÉ 2ļČäĻ░ä Ēæ£ļ®┤ņåīļÅģĒĢ£ ļīĆņøÉņĮ® ņóģņ×Éļź╝ 1ļ”Įņö® ĒīīņóģĒĢśņŚ¼ ņ×¼ļ░░ĒĢśņśĆļŗż. ņĮ®ņØś ņ┤łņāØņ×ÄņØ┤ ņÖäņĀäĒ׳ ņĀäĻ░£ļÉśĻ│Ā ņĀ£1ļ│ĖņŚĮņØ┤ ņČ£ĒśäĒĢś ņśĆņØä ļĢī, ņĀæņóģņøÉņ£╝ļĪ£ ņżĆļ╣äĒĢ£ ņØ┤ņæżņŗ£Ļ░£ļĪ£ ņ¦ĆņĀ£ļČĆĻ░Ć Ļ┤ĆĒåĄĒĢśļÅäļĪØ ņ░öļ¤¼ ļ│æņøÉĻĘĀņØä ņĀæņóģĒĢśĻ│Ā ļ®ĖĻĘĀĒĢ£ ņāüĒåĀļź╝ 1 cm Ļ░Ćļ¤ē ļŹ«ņ¢┤ņŻ╝ņŚłļŗż. ļ¼┤ņ▓śļ”¼ĻĄ¼ļŖö ļ│æņøÉĻĘĀņØä ņĀæņóģĒĢśņ¦Ć ņĢŖņØĆ ļ®ĖĻĘĀĒĢ£ ņØ┤ņæżņŗ£Ļ░£ļź╝ ņé¼ņÜ® ĒĢśņŚ¼ ļÅÖņØ╝ĒĢśĻ▓ī ņŗżĒŚśņØä ņłśĒ¢ēĒĢśņśĆļŗż. ļ│æņøÉĻĘĀņØä ņĀæņóģĒĢ£ ņĮ®ņØĆ 32┬░C ņØś ņāØņןņāü(Ļ┤æ/ņĢö, 12 hr/12 hr; ņŖĄļÅä, 50% ņØ┤ņāü)ņ£╝ļĪ£ ņś«Ļ▓© 30ņØ╝Ļ░ä ņ×¼ļ░░ĒĢśļ®░ ļ░£ļ│æņØä ņ£ĀļÅäĒĢśņśĆļŗż.
Ļ▓ĮĻĖ░ļÅä ĒÖöņä▒Ļ│╝ ņŚ░ņ▓£ņØś ļ│æļōĀ ņĮ®ņŚÉņä£ ļČäļ”¼ĒĢ£ HSW16-141, HSB16-159, HSS16-165ņÖĆ YSW16-175, YSB16-178, YSS16-176 ļō▒ ņ┤Ø 6ĻĘĀņŻ╝ļź╝ņäĀļ░£ĒĢśņŚ¼ ITS ņ£ĀņĀäņ×É ņŚ╝ĻĖ░ņä£ņŚ┤ ļČäņäØņØä ņŗżņŗ£ĒĢśņśĆļŗż. NucleoSpin PlantŌģĪ (MACHEREY-NAGEL, Duren, Germany) ĒéżĒŖĖļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ļÅÖĻ▓░Ļ▒┤ņĪ░ņŗ£Ēé© ļ│æņøÉĻĘĀņØś ĻĘĀņé¼ļĪ£ļČĆĒä░ genomic DNAļź╝ ņČöņČ£ ĒĢśĻ│Ā, ITS4 (5'-TCC TCC GCT TAT TGA TAT GC-3')Ļ│╝ ITS5 (5'-GGA AGT AAA AGT CGT AAC AAG G-3') ĒöäļØ╝ņØ┤ļ©Ėļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ITSņśüņŚŁņØä ņ”ØĒÅŁĒĢśņśĆļŗż. ņ£ĀņĀäņ×ÉņØś ņ”ØĒÅŁņØĆ 95┬░CņŚÉņä£ 4ļČä ņ▓śļ”¼ĒĢśĻ│Ā, 94┬░CņŚÉņä£ ļ│Ćņä▒ Ļ│╝ņĀĢ 30ņ┤ł, 48┬░CņŚÉņä£ Ļ▓░ĒĢ® Ļ│╝ņĀĢ 60ņ┤ł, 72┬░CņŚÉņä£ ņŗĀņן Ļ│╝ņĀĢ 60ņ┤łņØś ņŻ╝ĻĖ░ļź╝ ņ┤Ø 30ĒÜī ņŗżņŗ£ĒĢśņśĆņ£╝ļ®░, ļ¦łņ¦Ćļ¦ē ņŗĀņן Ļ│╝ņĀĢņØĆ 72┬░CņŚÉņä£ 7ļČäĻ░ä ņŗżņŗ£ĒĢśņśĆļŗż. ņ”ØĒÅŁļÉ£ PCR ņé░ļ¼╝ņØĆ 1.5% agarose gelņŚÉņä£ ņĀäĻĖ░ņśüļÅÖĒĢśņŚ¼ ļ░┤ļō£ļź╝ ĒÖĢņØĖĒĢśĻ│Ā, PCR purifica-tion kit (eCube PCR Purification Kit, Phile Korea, Seoul, Korea) ļź╝ ņØ┤ņÜ®ĒĢśņŚ¼ ņĀĢņĀ£ĒĢśņśĆļŗż. ņĀĢņĀ£ĒĢ£ DNAļŖö Macrogen (Seoul, Korea)ņŚÉ ņŚ╝ĻĖ░ņä£ņŚ┤ ļČäņäØņØä ņØśļó░ĒĢśņśĆņ£╝ļ®░, ļČäņäØļÉ£ ņŚ╝ĻĖ░ņä£ņŚ┤ņØĆnBLAST ĒöäļĪ£ĻĘĖļשņ£╝ļĪ£ GenBankņŚÉ ļō▒ļĪØļÉśņ¢┤ ņ׳ļŖö MacrophominaņåŹ Ļ│░ĒīĪņØ┤ ĻĘĀņŻ╝ņÖĆ ņĮ® ņłśĒÖĢĻĖ░ņŚÉ ļ░£ņāØĒĢśļŖö ņŗØļ¼╝ļ│æņØś ļ│æņøÉĻĘĀ ĻĘĀņŻ╝ņÖĆ ļ╣äĻĄÉĒĢśņśĆļŗż.
ļ░£ļ│æĒżņןņŚÉ ņŗ¼Ļ▓©ņ¦ä ļīĆņøÉņĮ®ņØä ņ£ĪņĢłņ£╝ļĪ£ ņĪ░ņé¼ĒĢśņŚ¼ Ļ▒┤ņĀäĒĢ£ ņĮ®Ļ│╝ ļ│æļōĀ ņĮ®ņ£╝ļĪ£ ĻĄ¼ļ│äĒĢśĻ│Ā, Ļ░üĻ░üņŚÉņä£ ņóģņ×Éļź╝ ņłśĒÖĢĒĢśņśĆļŗż. ņłśĒÖĢĒĢ£ ņóģņ×Éļź╝ ņŗżņś©ņŚÉņä£ 2ņŻ╝ņØ╝Ļ░ä Ļ▒┤ņĪ░ņŗ£Ēé©Ēøä, Ļ▒┤ņĀä ņĮ®Ļ│╝ ļ│æļōĀ ņĮ®ņØś 100ļ”Į ņżæĻ│╝ ņóģņ×ÉņØś ņ¦üĻ▓ĮņØä ņĪ░ņé¼ĒĢśņśĆļŗż.100ļ”Į ņżæņØĆ 10ļ░śļ│Ąņ£╝ļĪ£ ņĪ░ņé¼ĒĢśņśĆĻ│Ā, ņ¦üĻ▓ĮņØĆ 100ļ”ĮņØś ņóģņ×Éļź╝ 3ļ░śļ│Ąņ£╝ļĪ£ ņĪ░ņé¼ĒĢśņśĆļŗż.
ņĮ® ņ£Āļ¼śĻĖ░ņŚÉ ņ¦ĆņĀ£ļČĆņŚÉņä£ ņłśņ╣©ņāüņØś ļ│æņ¦ĢņØ┤ ĒśĢņä▒ļÉśļŗżĻ░Ć ļ¬©ņלļĪØ ņ”Øņāüņ£╝ļĪ£ ļ░£ņĀäĒĢśņśĆņ£╝ļ®░, ņČ£ņĢäĒĢ£ ļ¢Īņ×ÄņŚÉ Ļ▓ĆņØĆ ļ░śņĀÉņØ┤ļéśĒāĆļéśĻĖ░ļÅä ĒĢśņśĆļŗż(Fig. 1A, B). Ļ░£ĒÖöĻĖ░(2016ļģä 8ņøö 17ņØ╝)ņŚÉ ņ▒äņ¦æĒĢ£ ļ│æļōĀ ņĮ®ņØĆ ņ¦ĆņāüļČĆ ņ×ÄņØ┤ ĒÖ®ĒÖöļÉśĻĖ░ ņŗ£ņ×æĒĢśĻ│Ā ļČĆļČäņĀüņ£╝ļĪ£ Ļ░łļ│ĆĒĢśļŖö ļČĆņ£äļōżņØ┤ ļéśĒāĆļéśĻĖ░ ņŗ£ņ×æĒĢśņśĆļŗż(Fig. 2A). ņ▒äņ¦æĒĢ£ ļ│æļōĀ ņĮ®ņØś ļ┐īļ”¼ ņāØņ£ĪņØĆ ļ¦ÄņØ┤ ņ¢ĄņĀ£ļÉśņ¢┤ ņ׳ņŚłļŖöļŹ░, ņ×öļ┐īļ”¼Ļ░Ć ĒāłļØĮļÉśļ®░ļ┐īļ”¼ ļČĆņ£äņØś Ēæ£Ēö╝Ļ░Ć ļ▓ŚĻ▓©ņ¦Ćļ®┤ņä£ ĻĘĀĒĢĄņØ┤ ĒśĢņä▒ļÉśĻĖ░ ņŗ£ņ×æĒĢśņśĆļŗż(Fig. 2B). Ļ░£ĒÖöĻĖ░ ņØ┤Ēøä 9ņøö 12ņØ╝Ļ▓ĮņŚÉļŖö, ņ¦ĆņāüļČĆņŚÉ ļ¦łļ”ä ņ”ØņāüņØ┤ļÜ£ļĀĘĒĢśĻ▓ī ļéśĒāĆļéśĻĖ░ ņŗ£ņ×æĒĢśņśĆĻ│Ā, ļ┐īļ”¼Ļ│äņØś ņŻ╝ĻĘ╝ņØ┤ ņלļĀżļéśĻ░Ćļ®┤ņä£, Ļ│Āņé¼ĒĢśņśĆļŗż(Fig. 3). ļśÉĒĢ£ ņłśņ╣©ņāüņØś ņ”ØņāüņØä ļ│┤ņØ┤ļŹś ņżäĻĖ░ņŚÉļÅäņåīļ”ĮņØś ĻĘĀĒĢĄņØ┤ ĒśĢņä▒ļÉśņŚłļŗż. ņłśĒÖĢĻĖ░ņØĖ 10ņøö 12ņØ╝ Ļ▓ĮņŚÉ ļ│æņ¦ĢņØä ļ│┤ļ®┤, Fig. 4ņŚÉņä£ ļ│┤ļŖö Ļ▓āĻ│╝ Ļ░ÖņØ┤ ņøÉĻ▒░ļ”¼ņØś ĒżņןņŚÉņä£ļÅä ļ¦łļ”ä ņ”ØņāüņØ┤ ļéśĒāĆļé£ ļČĆņ£äĻ░Ć ļÜ£ļĀĘĒĢśĻ▓ī ĻĄ¼ļ│äļÉśņŚłļŗż. ļśÉĒĢ£ ļ│æļōĀ ņĮ®ņØś ņżäĻĖ░ Ēæ£ļ®┤Ļ│╝ ņ¦ĆņĀ£ļČĆņØś Ēæ£Ēö╝Ļ░Ć ļ▓ŚĻ▓©ņ¦ä ļé┤ļČĆ Ēö╝ņĖĄ ļČĆņ£äņŚÉ ĒśĢņä▒ļÉ£ ĻĘĀĒĢĄņØäļÜ£ļĀĘĒĢśĻ▓ī Ļ┤Ćņ░░ĒĢĀ ņłś ņ׳ņŚłļŗż. ļ│æļōĀ Ļ░£ņ▓┤ņØś ņżäĻĖ░ļź╝ ņäĖļĪ£ļĪ£ ņĀłļŗ©ĒĢĀ Ļ▓ĮņÜ░ ņ£ĀĻ┤ĆņåŹ ļČĆņ£äņŚÉ ļŗżļ¤ēņØś ĻĘĀĒĢĄņØ┤ ĒśĢņä▒ļÉ£ Ļ▓āņØä ļ│╝ ņłś ņ׳ņŚłļŗż (Fig. 4). ņĮ®ņŚÉņä£ņØś ļ│æņ¦ĢņØĆ M. phaseolinaĻ░Ć ļĖöļŻ©ļ▓Āļ”¼ļź╝ ņ╣©ņ×ģĒĢĀ ļĢī ņ¦ĆņāüļČĆņØś ņ×ÄņØ┤ ņŗ£ļōżĻ│Ā, ņżäĻĖ░ņÖĆ ļ┐īļ”¼ļŖö Ļ░łļ│ĆĒĢśļ®┤ņä£ ņŗ£ļō£ļŖö ņ”ØņāüĻ│╝ ņ£Āņé¼ĒĢśņśĆļŗż(de los Santos ļō▒, 2019).Ļ▓░ĻĄŁ, ĒżņןņŚÉņä£ M. phaseolinaĻ░Ć ņĮ®ņØä ņ╣©ņ×ģĒĢśĻ▓ī ļÉśļ®┤ ņĮ®ņ×ÄņØ┤ ņŗ£ļōżļ®┤ņä£ ņĪ░ĻĖ░ņŚÉ ņćĀņĢĮĒĢ┤ņ¦ĆĻ│Ā ņŗØļ¼╝ņ▓┤Ļ░Ć ņØĆĒÜīņāēņ£╝ļĪ£ ļ│ĆņāēļÉśņ¢┤ ņŻĮņŚłļŗż. ņ┤łĻĖ░ņŚÉļŖö ļ┐īļ”¼, ņ¦ĆņĀ£ļČĆ, ņżäĻĖ░ņŚÉ ņłśņ╣©ņāüņØś ņ”ØņāüņØ┤ ļéśĒāĆļéśļ®░, ļ│æņØ┤ ņ¦äņĀäļÉśļ®┤ņä£ ļ┐īļ”¼ņÖĆ ņ¦ĆņĀ£ļČĆņØś Ēæ£Ēö╝ņĪ░ņ¦üņØ┤ ļ▓ŚĻ▓©ņ¦ĆĻ│Ā, ĻĘĖ ņåŹņŚÉ Ļ▓ĆņØĆņāēņØś ņåīļ”ĮĻĘĀĒĢĄņØ┤ ĒśĢņä▒ļÉśĻĖ░ ņŗ£ņ×æĒĢśņśĆļŗż. ņĮ®ņØś ĒÆłņóģņŚÉ ļö░ļØ╝ņä£ Ēæ£Ēö╝Ļ░Ć Ēä░ņ¦Ćļ®┤ņä£ ņä¼ņ£ĀņĪ░ņ¦üņØ┤ Ļ░łļØ╝ņ¦ĆļŖö ņ”ØņāüņØ┤ ļéśĒāĆļéśĻĖ░ļÅä ĒĢśņśĆļŗż. ņØ┤ļ¤¼ĒĢ£ ļ│æņ¦ĢņØä ļ│┤ņØ┤ļŖö ĻĖ░ņŻ╝ļŖö Ļ▒┤ņĀäĒĢ£ ņĮ®Ļ│╝ļŖö ļŗżļź┤Ļ▓ī ļ┐īļ”¼ņÖĆ ņ¦ĆņĀ£ļČĆĻ░Ć ņŹ®Ļ│Ā ņ×öļ┐īļ”¼Ļ░Ć Ļ▒░ņØś ņŚåņ¢┤ ņל ļĮæĒ׳ļ®░, Ļ╝¼Ēł¼ļ”¼Ļ░Ć ņĀ£ļīĆļĪ£ ņŚ¼ļ¼╝ņ¦Ć ņĢŖņĢä ļīĆļČĆļČä Ļ▓░ņŗżņØ┤ ļÉśņ¦Ć ņĢŖņĢśļŗż.
ļ│æļōĀ ņĮ® ņĪ░ņ¦üņŚÉņä£ ļ│æņøÉĻĘĀņØä ļČäļ”¼ĒĢ£ Ļ▓░Ļ│╝, Macrophomina, Phomopsis, Colletotrichum, Botryospaeria, CercosporaņåŹņØś ņŗØļ¼╝ļ│æņøÉĻ│░ĒīĪņØ┤Ļ░Ć ļČäļ”¼ļÉśņŚłņ£╝ļ®░, MacrophominaņØś ļČäļ”¼ļ╣łļÅäļŖö 15.2%ņØ┤ņŚłļŗż(Table 1). ņĮ® ņØ┤ņÖĖņŚÉļÅä ņ░Ė Ļ╣©ņÖĆ ĒīźņŚÉņä£ MacrophominaļŖö Ļ░üĻ░ü 26.7%ņÖĆ 9.1%ņö® ļČäļ”¼ļÉśņŚłļŗż. ĒĢśņ¦Ćļ¦ī ņĮ® ņØ┤ņÖĖņØś ņ×æļ¼╝ņØĆ ņ▒äņ¦æĒĢ£ ņŗ£ļŻīņØś ņłśĻ░Ć ņĀüņŚłļŹś Ļ┤ĆĻ│äļĪ£ ļŹö ņäĖļ░ĆĒĢ£ ņĪ░ņé¼ļź╝ ņŗżņŗ£ĒĢĀ ĒĢäņÜöĻ░Ć ņ׳ļŗż.
ļČäļ”¼ĒĢ£ ļ│æņøÉĻĘĀ M. phaseolina HSW16-141 ĻĘĀņŻ╝ļź╝ 30┬░CņØś PDA ļ░░ņ¦ĆņŚÉņä£ ļ░░ņ¢æĒĢśļ®┤ ĻĘĀņ┤ØņØś ĻĘĀņé¼ ņāēĻ╣öņØ┤ ņ▓śņØīņŚÉļŖö ĒØ░ņāēņØä ļØäļŗżĻ░Ć ļ░░ņ¢æĻĖ░Ļ░äņØ┤ Ļ▓ĮĻ│╝ĒĢśļ®┤ņä£ ĒÜīņāē ļé┤ņ¦Ć Ļ▓ĆņØĆņāēņ£╝ļĪ£ ļ│ĆĒĢśņśĆļŗż. ļ░░ņ¢æĒĢśĻ│Ā 5ņØ╝ņØ┤ ņ¦Ćļéśļ®┤ņä£ļČĆĒä░ PDA ļ░░ņ¦Ć ņāüņŚÉņä£ Ļ▓ĆņĀĢņāēņØś ĻĄ¼ĒśĢņØĖ ņåīļ”ĮĻĘĀĒĢĄņØ┤ ĒśĢņä▒ļÉśĻĖ░ ņŗ£ņ×æĒĢśņśĆņ£╝ļ®░, ĒÅēĻĘĀ ņ¦üĻ▓ĮņØĆ 91 ┬Ąm (ņ¦üĻ▓Į ļ▓öņ£ä, 61-124 ┬Ąm)ņØ┤ņŚłļŗż. ļĖöļŻ©ļ▓Āļ”¼ņØś ļ│æļōĀ ņĪ░ņ¦üņŚÉņä£ ļČäļ”¼ĒĢ£ ļ│æņøÉĻĘĀļÅä 30┬░CņØś ņĢöņāüĒā£ņŚÉņä£ ļ░░ņ¢æĒĢśļ®┤ Ļ▓ĆĻ│Ā ļæźĻĘ╝ ņåīļ”ĮĻĘĀĒĢĄņØä ĒśĢņä▒ĒĢśļŖöļŹ░, ņåīļ”ĮĻĘĀĒĢĄņØś Ēü¼ĻĖ░ļŖö ĒÅēĻĘĀ 98 ┬Ąm (61-128 ┬Ąm)ļĪ£ ņĮ®ņŚÉņä£ ļČäļ”¼ĒĢ£ ņåīļ”ĮĻĘĀĒĢĄĻ│╝ ĒśĢĒā£ņĀüņ£╝ļĪ£ ļ¦żņÜ░ ņ£Āņé¼ĒĢśņśĆļŗż(de los Santos ļō▒, 2019). ļČäņāØĒżņ×ÉņÖĆ ļČäņāØĒżņ×ÉĻ░üņØĆ PDA ļ░░ņ¦ĆņāüņŚÉņä£ļŖö ĒśĢņä▒ļÉśņ¦Ć ņĢŖņĢśļŗż. ĒĢśņ¦Ćļ¦ī ļ®ĖĻĘĀĒĢ£ ļ│┤ļ”¼ ņ×ÄņØä ļ¼╝ĒĢ£ņ▓£ ļ░░ņ¦Ć ņ£äņŚÉ ņś¼ļĀżļåōĻ│Ā ļ│┤ļ”¼ņ×Ä ņ£äņŚÉ M. phaseolina HSW16-141ņØä ņĀæņóģĒĢśņŚ¼ ļ░░ņ¢æĒĢśņśĆņØä ļĢī, Ļ▓ĆņĀĢņāēņØś ļæźĻĘ╝ ļČäņāØĒżņ×ÉĻ░üņØ┤ ĒśĢņä▒ļÉśņŚłņ£╝ļ®░, ļČäņāØĒżņ×ÉĻ░ü ņĢłņŚÉļŖö ļüØņØ┤ ļæźĻĖĆĻ│Ā ĒāĆņøÉĒśĢņØ┤ļ®░ Ēł¼ļ¬ģĒĢ£ ļŗ©Ēżņ×ÉņØĖ ļČäņāØĒżņ×ÉĻ░Ć ļīĆļ¤ēņ£╝ļĪ£ ĒśĢņä▒ļÉśņŚłļŗż(Fig. 5). ļČäņāØĒżņ×ÉĻ░üņØś ĒÅēĻĘĀ ņ¦üĻ▓ĮņØĆ 221 ┬Ąm (157-301 ┬Ąm)ņØ┤ņŚłņ£╝ļ®░, ļČäņāØĒżņ×ÉņØś ņןĻ▓ĮĻ│╝ ļŗ©Ļ▓Į ņØĆ 24 ┬Ąm (16-33 ┬Ąm)ņÖĆ 11 ┬Ąm (9-13 ┬Ąm)ņØ┤ņŚłļŗż. ļ│┤ļ”¼ņ×ÄņŚÉņä£ļÅä Ļ▓ĆņĀĢņāēņØś ĻĄ¼ĒśĢņØĖ ņåīļ”ĮĻĘĀĒĢĄņØ┤ ĒśĢņä▒ļÉśņŚłļŗż.
M. phaseolina HSW16-141ņØä PDA ļ░░ņ¦ĆņŚÉ ņĀæņóģĒĢśĻ│Ā Ļ░üĻ░üņØś ņś©ļÅäņŚÉņä£ 2ņØ╝Ļ░ä ļ░░ņ¢æĒĢ£ Ēøä ĻĘĀņ┤ØņØś ņ¦üĻ▓ĮņØä ņĪ░ņé¼ĒĢ£ Ļ▓░Ļ│╝, 35┬░CņŚÉ ņä£ 8.2 cmļĪ£ Ļ░Ćņן ļ╣Āļź┤Ļ▓ī ņāØņןĒĢśņśĆĻ│Ā, 30┬░CņÖĆ 37┬░CņŚÉņä£ļŖö 6.1 Ļ│╝ 6.3 cmļĪ£ ņāØņן ņåŹļÅäĻ░Ć ņĀĆĒĢśļÉśņŚłļŗż. ņØ╝ļ░śņĀüņØĖ ņŗØļ¼╝ļ│æņøÉĻ│░ĒīĪ ņØ┤ņØś ņāØņן ņĀüņś©ņ£╝ļĪ£ ņĢīļĀżņ¦ä 20┬░C, 25┬░C, 28┬░CņŚÉņä£ ĻĘĀņé¼ ņāØņן ņĀĢļÅäļŖö 4.1, 5.0, 5.6 cmļĪ£ ņĀĆņĪ░ĒĢśņśĆļŗż(Fig. 6). ņżæĻĄŁņØś faba beanņŚÉ ņä£ ļČäļ”¼ĒĢ£ M. phaseolina FMP8-1, FMP8-2, FMP8-4ņÖĆ Ļ░ÖņØĆ ĻĘĀņŻ╝ļŖö ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ ņé¼ņÜ®ĒĢ£ ņĮ®ņŚÉņä£ ļČäļ”¼ĒĢ£ ĻĘĀņŻ╝ņÖĆļŖö ļŗżļź┤Ļ▓ī 28┬░ CņØś PDA ļ░░ņ¦ĆņŚÉņä£ 12ņŗ£Ļ░ä Ļ┤æņØä ņĪ░ņé¼ĒĢśļ®░ ļ░░ņ¢æĒĢśņśĆņØä ļĢī ņāØņן ņØ┤ ļ╣©ļ×Éļŗż(Sun ļō▒, 2019). ņØ┤ļ¤░ Ļ▓░Ļ│╝ļź╝ ļ│┤ļ®┤ ĻĄŁļé┤ņŚÉņä£ ļČäļ”¼ĒĢśļŖö M. phaseolinaņØś ņāØļ”¼ŃåŹņ£ĀņĀäņĀüņØĖ ļŗżņ¢æņä▒ņØä ņĪ░ņé¼ĒĢ┤ņĢ╝ ĒĢĀ ĒĢäņÜöņä▒ņØ┤ ņ׳ļŗżĻ│Ā ņāØĻ░üĒĢ£ļŗż.
ITS ņŚ╝ĻĖ░ņä£ņŚ┤ ļČäņäØņØä ņ£äĒĢ┤ņä£ ITS4ņÖĆ ITS5 ĒöäļØ╝ņØ┤ļ©ĖļĪ£ M. phaseolina ĻĘĀņŻ╝ļōżņØś ņ£ĀņĀäņ×Éļź╝ ņ”ØĒÅŁĒĢśņŚ¼ 580 bpņØś ņ”ØĒÅŁņé░ļ¼╝ņØä ņ¢╗ņŚłļŗż. CummingsņÖĆ Bergstrom (2013) ņØĆ ļ»ĖĻĄŁ ļē┤ņÜĢņŻ╝ņŚÉņä£ ņĮ®ņŚÉ charcoal rot ņ”ØņāüņØä ņØ╝ņ£╝ĒéżļŖö Mp001NY12 ĻĘĀņŻ╝ļĪ£ļČĆĒä░ ITS1Ļ│╝ ITS4 ĒöäļØ╝ņØ┤ļ©Ėļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ITS ņśüņŚŁņØś ņ£ĀņĀäņ×Éļź╝ ņ”ØĒÅŁĒĢśĻ│Ā ņŚ╝ĻĖ░ņä£ņŚ┤ņØä ļČäņäØĒĢ£ Ļ▓░Ļ│╝, M. phaseolinaņÖĆ 100% ņØ╝ņ╣śĒĢśņśĆļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż. Sun ļō▒(2019)ļÅä ņŚŁņŗ£ faba beanņŚÉņä£ ļéśĒāĆļéśļŖö charcoal rotņØś ņøÉņØĖĻĘĀņØä ļČäļ”¼ĒĢśņŚ¼ ņ£ĀņĀäņ×É ņłśņżĆņŚÉņä£ ļÅÖņĀĢņØä ņŗżņŗ£ĒĢśņśĆļŖöļŹ░, ITS4ņÖĆ ITS5 ĒöäļØ╝ņØ┤ļ©Ėļź╝ ņé¼ņÜ®ĒĢśņŚ¼ ņĢĮ 600 bpņØś ITS ņśüņŚŁ ņ£ĀņĀäņ×Éļź╝ ņ”ØĒÅŁĒĢśņśĆņ£╝ļ®░, ņØ┤ ņé░ļ¼╝ņØś ņŚ╝ĻĖ░ņä£ņŚ┤ņØä ļČäņäØĒĢ£ Ļ▓░Ļ│╝, M. phaseolinaņÖĆ 99-100% ņØ╝ņ╣śĒĢśņśĆļŗż. ļ│Ė ņŚ░ĻĄ¼ņŚÉņä£ļÅä ņĮ®ņŚÉņä£ ļČäļ”¼ĒĢ£ 6ĻĘĀņŻ╝ņØś ITS ņśüņŚŁ ņŚ╝ĻĖ░ ņä£ņŚ┤ņØä NCBIņØś GenBankņŚÉ ļō▒ļĪØļÉ£ M. phaseolinaņØś ņŚ╝ĻĖ░ņä£ņŚ┤Ļ│╝ ļ╣äĻĄÉĒĢ£ Ļ▓░Ļ│╝, 100% ņØ╝ņ╣śĒĢśņśĆļŗż. M. phaseolinaņØś ITS ņŚ╝ĻĖ░ņä£ ņŚ┤ņØś Ļ│äĒåĄļČäņäØņØä ĒåĄĒĢ┤ņä£ M. phaseolinaļŖö Botryosphaeriaceae Ļ│╝ņŚÉ ņåŹĒĢśļŖö Botryosphaeria sp.ņÖĆļŖö ĻĘ╝ņŚ░Ļ┤ĆĻ│äņŚÉ ņ׳ņ£╝ļéś, ņĮ® ņłśĒÖĢĻĖ░ņŚÉ ļ░£ņāØĒĢśļŖö Diaporthe, Colletotrichum, Calonectira ļō▒Ļ│╝ ļŖö ļÜ£ļĀĘĒĢ£ ņ░©ņØ┤Ļ░Ć ņ׳ņØīņØä ņĢī ņłś ņ׳ņŚłļŗż(Fig. 7).
ļ│æņøÉĻĘĀņØä ņĀæņóģĒĢśņŚ¼ ņżĆļ╣äĒĢ£ ņØ┤ņæżņŗ£Ļ░£ļź╝ ņØ┤ņÜ®ĒĢ£ ņāüņ▓ś ņĀæņóģņŚÉņä£ ņĮ®ņØĆ ņĀæņóģĒĢ£ ņ¦Ć 45ņØ╝Ļ▓ĮļČĆĒä░ ļ│æņ¦ĢņØ┤ ļéśĒāĆļé¼ļŗż. ĒżņןņŚÉņä£ Ļ┤Ćņ░░ĒĢ£ ļ░öņÖĆ Ļ░ÖņØ┤ ņĮ®ņØś ņ¦ĆņĀ£ļČĆņŚÉ ņłśņ╣©ņāü ļ│æņ¦ĢņØ┤ ļéśĒāĆļéśļŗżĻ░Ć Ļ░łņāē ļé┤ņ¦Ć Ļ▓ĆņØĆņāēņ£╝ļĪ£ ļ│ĆņāēļÉśĻĖ░ ņŗ£ņ×æĒĢśņśĆņ£╝ļ®░, ļ│æņØ┤ ņ¦äĒ¢ēļÉśļ®┤ņä£ ņĮ®ņØś ņżäĻĖ░ņŚÉņä£ Ļ▓ĆņØĆņāēņØś ņåīļ”ĮĻĘĀĒĢĄņØ┤ ĒśĢņä▒ļÉśņŚłĻ│Ā Ļ▓░ĻĄŁ ņŗ£ļōżņ¢┤ Ļ│Āņé¼ĒĢśņśĆļŗż. ļśÉĒĢ£ ļ│æļōĀ ļČĆņ£äņŚÉņä£ ņĀæņóģĒĢ£ ļ│æņøÉĻĘĀĻ│╝ ļÅÖņØ╝ĒĢ£ M. phaseolinaļź╝ ņ×¼ļČäļ”¼ĒĢĀ ņłś ņ׳ņŚłļŗż(Fig. 8).
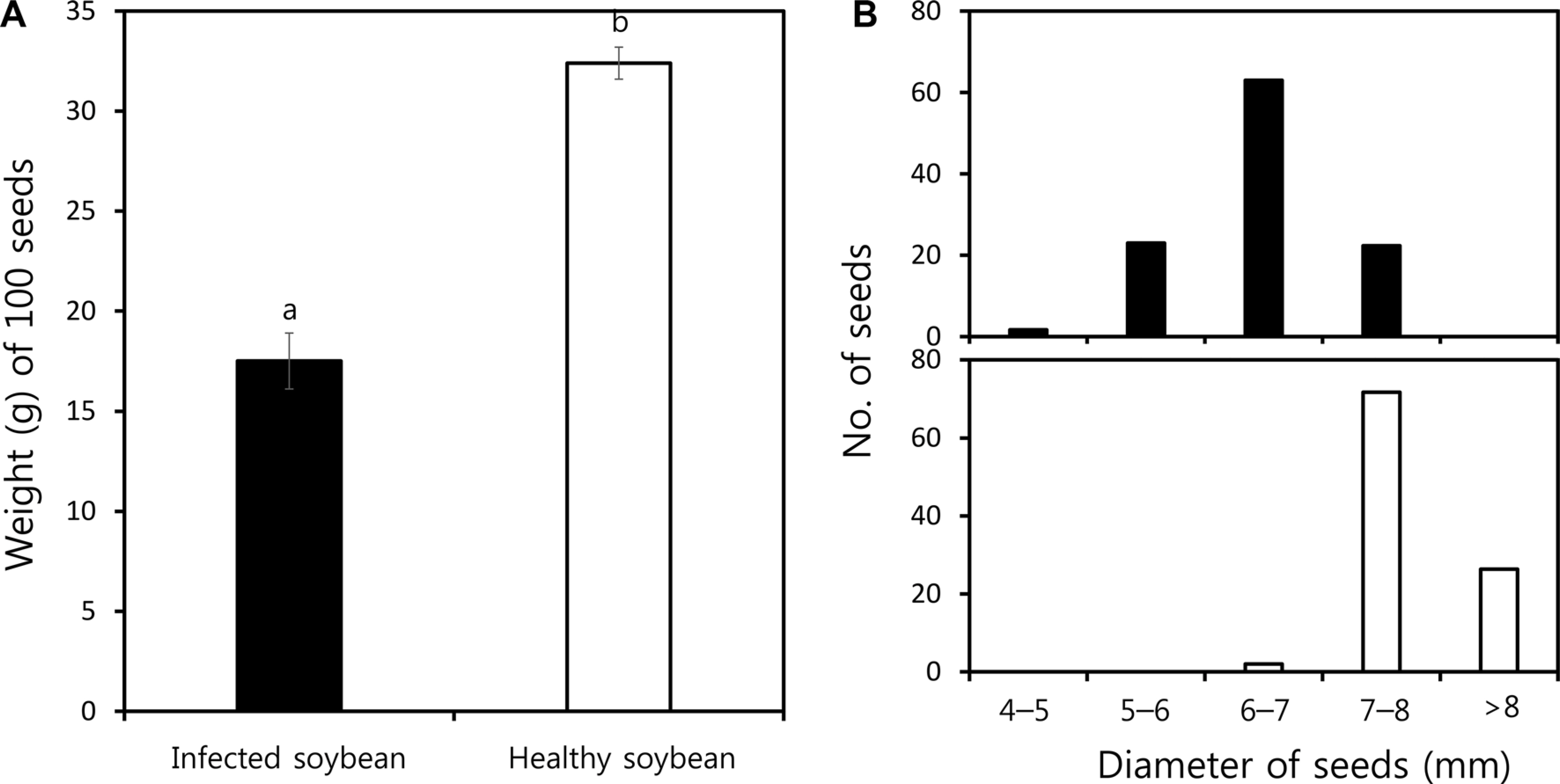
M. phaseolinaĻ░Ć ņ╣©ņ×ģĒĢśņŚ¼ ļ│æņØ┤ ļ░£ņāØĒĢĀ Ļ▓ĮņÜ░ ņĮ®ņØś ņłśĒÖĢļ¤ēĻ│╝ ĒÆłņ¦łņØ┤ ĒśäņĀĆĒĢśĻ▓ī Ļ░ÉņåīĒĢśņśĆļŗż. ļīĆņøÉņĮ® ņØä ņłśĒÖĢĒĢ£ Ēøä, Fig. 9ņŚÉņä£ ļ│┤ļŖö Ļ▓āĻ│╝ Ļ░ÖņØ┤ Ļ▒┤ņĀäĒĢ£ ņĮ® ņóģņ×ÉņÖĆ ļ│æ 10A).ĒĢ┤ņä£ ņĮ® ņóģņ×ÉņØśņ¦üĻ▓ĮņØä ņĪ░ņé¼ĒĢśņśĆļŗż. Ļ▒┤ņĀäĒĢ£ ņĮ® ņóģņ×ÉļŖö ņ¦üĻ▓ĮņØ┤ 8 mm ņØ┤ņāü ņóģņ×ÉĻ░Ć 26%, 7 mm ņØ┤ņāüļČĆĒä░ 8 mm ņØ┤ĒĢśĻ░Ć 72%, 6 mm ņØ┤ņāüņØ┤Ļ│Ā 7mm ņØ┤ĒĢśņØĖ ņóģņ×ÉĻ░Ć 2%ņØĖļŹ░ ļ╣äĒĢśņŚ¼, ļ│æļōĀ ņĮ® ņóģņ×ÉņØś Ļ▓ĮņÜ░ņŚÉļŖö 8mm ņØ┤ņāüņØĖ ņóģņ×ÉļŖö ņŚåĻ│Ā 7 mm ņØ┤ņāüņØ┤ļ®░ 8 mm ņØ┤ĒĢśņØĖ ņóģņ×ÉĻ░Ć12%, 6 mm ņØ┤ņāüņØ┤ļ®░ 7 mm ņØ┤ĒĢśņØĖ Ļ▓āņØ┤ 63%, 5 mm ņØ┤ņāüņØ┤ļ®░6 mm ņØ┤ĒĢśņØĖ Ļ▓āņØ┤ 23%, ĻĘĖļ”¼Ļ│Ā 4 mm ņØ┤ņāüņØ┤ļ®░ 5 mm ņØ┤ĒĢśņØĖ ņóģņ×ÉļÅä 2%ļéś ļÉśņŚłļŗż(Fig. 10B). ņØ┤ņ▓śļ¤╝ M. phaseolinaļŖö ņĮ®ņØś ņāØ ņé░ļ¤ēļ┐Éļ¦ī ņĢäļŗłļØ╝ ņłśĒÖĢĒĢ£ ņĮ®ņØś ĒÆłņ¦łņŚÉļÅä ņśüĒ¢źņØä ļ»Ėņ│żļŗż. ĻĄŁļé┤ņŚÉņä£ļŖö YuņÖĆ Park (1980)ņØ┤ ņ░ĖĻ╣© ņóģņ×ÉņŚÉņä£ ļČäļ”¼ĒĢ£ M. phaseolinaņØś ļ│æņøÉņä▒ņØä ļ│┤Ļ│ĀĒĢśņśĆņ£╝ļ®░, Sung ļō▒(1980)ņØĆ ļ│æļōĀ ņĮ®ņØś ņżäĻĖ░ļéś ļ┐īļ”¼ņŚÉņä£ M. phaseolinaļź╝ ļČäļ”¼ĒĢśĻ│Ā ņĮ®ņŚÉ ļīĆĒĢ£ ļ│æņøÉņä▒ņØä ĒÖĢņØĖĒĢśņśĆļŗż. YuņÖĆ Park (1982)ņØĆ ĒĢ£ĻĄŁņé░ ņŻ╝ņÜöņ×æļ¼╝ņŚÉņä£ ņóģņ×ÉņĀäņŚ╝ņä▒ ņ¦äĻĘĀņŚÉ ļīĆĒĢ┤ ņĪ░ņé¼ļź╝ ņŗżņŗ£ĒĢśļ®┤ņä£ ņ░ĖĻ╣© ņŗ£ļŻīņŚÉņä£ 0.5-8.5% ļ╣äņ£©ļĪ£ M. phaseolinaļź╝ Ļ▓ĆņČ£ĒĢśņśĆņ£╝ļ®░, YumĻ│╝ Park (1989)ņØĆ Ļ▓ĆņØĆņĮ®ņ£╝ļĪ£ļČĆĒä░ ĒÅēĻĘĀ 0.08%ļĪ£ M. phaseolinaļź╝ Ļ▓ĆņČ£ ĒĢśņśĆļŗżĻ│Ā ļ│┤Ļ│ĀĒĢśņśĆļŗż. M. phaseolinaļŖö ņóģņ×ÉņĀäņŚ╝Ļ│╝ ĒåĀņ¢æņĀäņŚ╝ņØä ĒĢśĻ│Ā, ĒåĀņ¢æ ņåŹņŚÉņä£ 2-15ļģä ļÅÖņĢł ņāØņĪ┤ņØ┤ Ļ░ĆļŖźĒĢśļ®░(Short ļō▒, 1980), ņåīļ”ĮĻĘĀĒĢĄņØĆ ņØ╝ņ░© ņĀäņŚ╝ņøÉņØś ņŚŁĒĢĀņØä ĒĢ£ļŗżĻ│Ā ņĢīļĀżņĀĖ ņ׳ļŗż (Gupta ļō▒, 2012; Kaur ļō▒, 2012). ļö░ļØ╝ņä£ ņĄ£ĻĘ╝ ļōżņ¢┤ ĻĄŁļé┤ ņĮ® ņ×¼ļ░░ ĒżņןņŚÉņä£ ļ░£ņāØĒĢśļŖö M. phaseolinaņŚÉ ņØśĒĢ£ ļ│æņØĆ ļ│æņøÉĻĘĀņØ┤ ņØ┤ļ»Ė ĒåĀņ¢æ ņåŹņŚÉ ņĪ┤ņ×¼ĒĢśĻ│Ā ņ׳ņŚłņ£╝ļ®░, ņĄ£ĻĘ╝ ļ│æņøÉĻĘĀņØś ņāØņןņŚÉ ņĀüĒĢ®ĒĢ£ Ļ│Āņś© Ļ▒┤ņĪ░ĒĢ£ ļéĀņö©Ļ░Ć ņ¦ĆņåŹļÉśļ®┤ņä£ ļ│æņØ┤ ļ░£ņāØĒĢ£ Ļ▓āņ£╝ļĪ£ ĒīÉļŗ©ļÉśņ¢┤ņ¦äļŗż. ņØ┤ļ»Ė ņśżļל ņĀäņŚÉ YumĻ│╝ Park (1989)ņØ┤ M. phaseolinaņØś ņóģņ×É ņĀäņŚ╝ņØä ļ│┤Ļ│ĀĒĢśņśĆĻ│Ā, ņÜöņ”łņØī ļ│ĆĒÖöĒĢśļŖö ĻĖ░ņāü ņĪ░Ļ▒┤ņ£╝ļĪ£ ņØĖĒĢśņŚ¼ ĒżņןņŚÉņä£ M. phaseolinaņŚÉ ņØśĒĢ£ ļ│æ ļ░£ņāØņØ┤ ņ”ØĻ░ĆĒĢśĻ│Ā ņ׳ļŖö Ļ▓āņØä ļ│┤ļ®┤, ĒżņןņŚÉņä£ ļ░£ņāØ ņ£Āļ¼┤ņÖĆ ļ│æņøÉĻĘĀņØś ļČäĒż, ĻĘĖļ”¼Ļ│Ā ļ│æ ļ░£ņāØ ņāØĒā£ ļō▒ņŚÉ ļīĆĒĢ£ Ē¢źĒøä ņĪ░ņé¼Ļ░Ć ĒĢäņÜöĒĢĀ ļ┐Éļ¦ī ņĢäļŗłļØ╝, ņĮ® ņóģņ×ÉņØś ņāØņé░Ļ│╝ ļ│┤ĻĖē ņĖĪļ®┤ņŚÉņä£ļÅä ļ¦ÄņØĆ ņŻ╝ņØśĻ░Ć ĒĢäņÜöĒĢ£ ņāüĒā£ņØ┤ļŗż.ņØ┤ņāüņØś Ļ▓░Ļ│╝ņŚÉņä£ ļ│┤ļŖö Ļ▓āĻ│╝ Ļ░ÖņØ┤ ņĄ£ĻĘ╝ ĻĖ░Ēøäļ│ĆĒÖöņŚÉ ļö░ļźĖ Ļ│Āņś© Ļ▒┤ņĪ░ĒĢ£ ņĪ░Ļ▒┤ņŚÉņä£ ņĮ®ņŚÉ ļéśĒāĆļéśļŖö ļ¦łļ”ä ņ”ØņāüņØ┤ M. phaseolinaņŚÉ ņØśĒĢ£ Ļ▓āņ×äņØä ļ│┤Ļ│ĀĒĢśļ®┤ņä£, ņĮ®ņŚÉņä£ ļ░£ņāØĒĢ£ M. phaseolinaņŚÉ ņØśĒĢ£ ļ¦łļ”ä ņ”ØņāüņØä ņĮ® ĻĘĀĒĢĄļ¦łļ”äļ│æņ£╝ļĪ£ ļ¬ģļ¬ģĒĢśĻ│Āņ×É ĒĢ£ļŗż.
Acknowledgments
This research was carried out with support from the Rural Development Administration project (project title; Investigation of plant diseases caused by Macrophomina sp. and classification and identification of pathogen through DNA sequence analysis (PJ014956022020)), and we appreciate the support.
Fig.┬Ā1
Damping off in soybean. (A) Water-soaked symptoms near the soil ground of soybean seedlings. (B) Damping off in soybean seedlings and black spots on cotyledon leaves.

Fig.┬Ā2
Diseased soyeans collected during the flowering period. (A) Diseased soybeans collected during the flowering period began to yellowing in the ground leaves and partially browning areas appeared. (B) The growth of the roots of the diseased soybeans was largely suppressed. As the roots were eliminated, the epidermis of the roots was peeled off, and the sclerotia formed. The arrow points to the root part where the epidermis is peeled off.

Fig.┬Ā3
Blight symptom of soybean. Soybeans began to show the blight throughout the plant (A), and tap root were cut off and died (B, C).

Fig.┬Ā4
Soybean field (A) where beans are dead due to blight and symptoms in the late growth period (B-D). It was easy to see that some of the soybean fields were dying from dryness. Sclerotia formed on the stem surface of the diseased soybean and on the inner cortex where the epidermis of the stem was stripped were clearly observed.

Fig.┬Ā5
Macrophomina phaseolina produced on barley leaves on an water agar medium. (A) Conidia and pycnidium on a barley leaf (├Ś200). (B) Pycnida and macrosclerotia formed in water agar leaf medium (├Ś45).
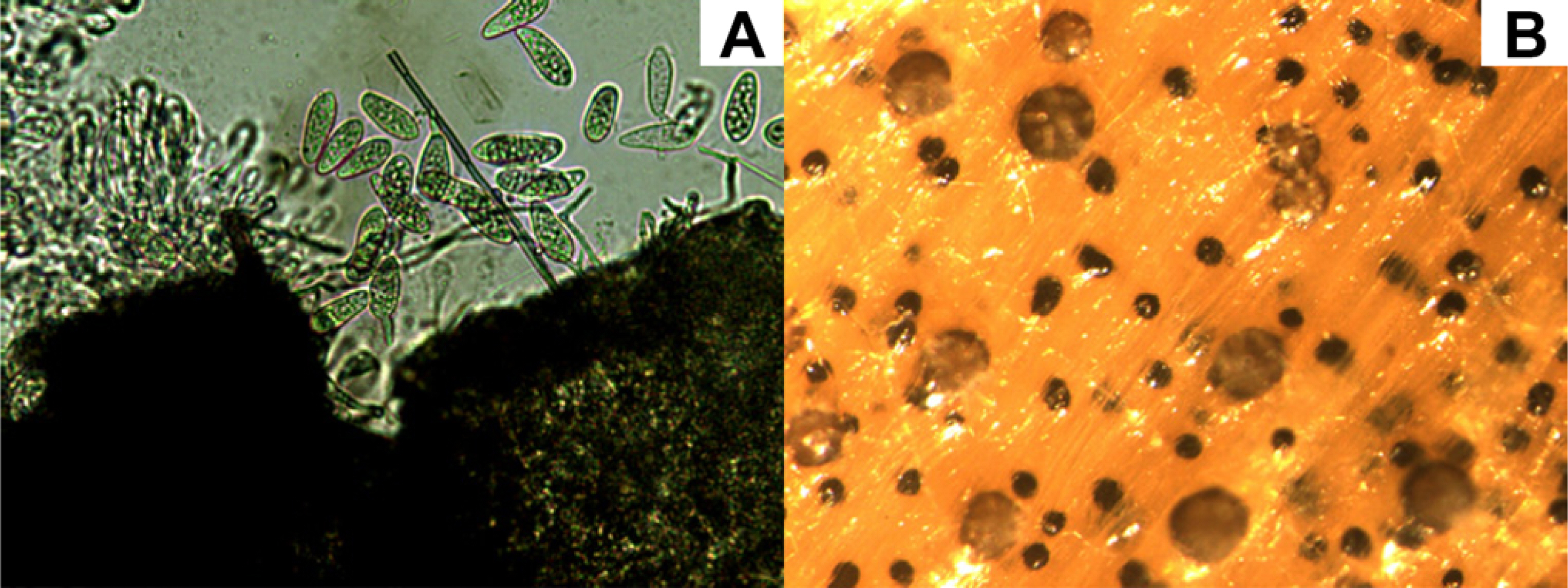
Fig.┬Ā6
Mycelial growth of Macrophomina phaseolina isolated from infected soybean plants on potato dextrose agar at indicated temperatures. Colony diameter was measured after incubation for 2 days under the dark condition. The colony diameter was the average of three replications. The different letters on the bars are statistically significant based on Duncan multiple range test (PŌēż0.01).
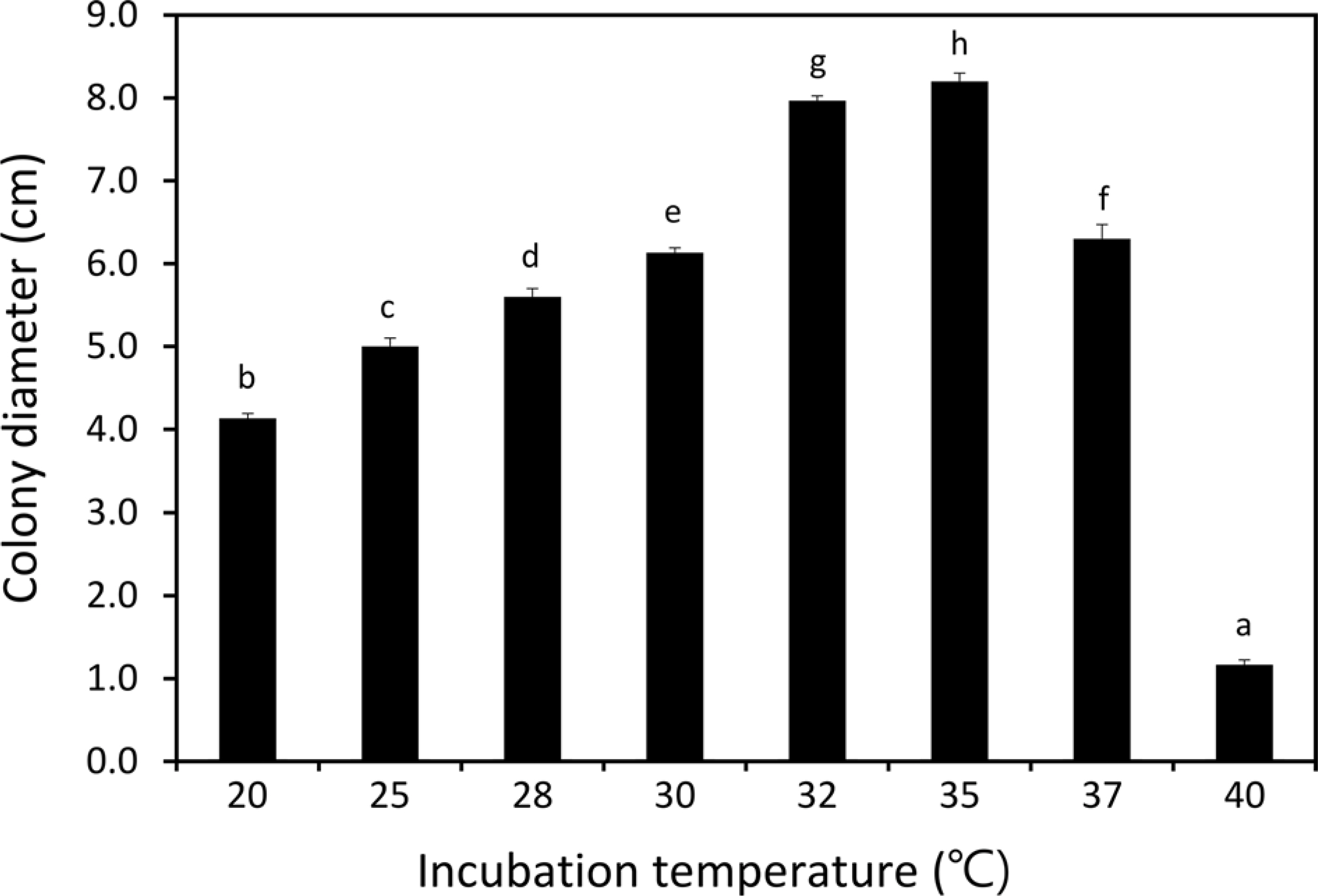
Fig.┬Ā7
Phylogenetic tree of the Macrophomina phaseolina isolates constructed from the multiple alignments of internal transcribed spacer rDNA sequences, using neighbour-joining method and 2,000 boots.
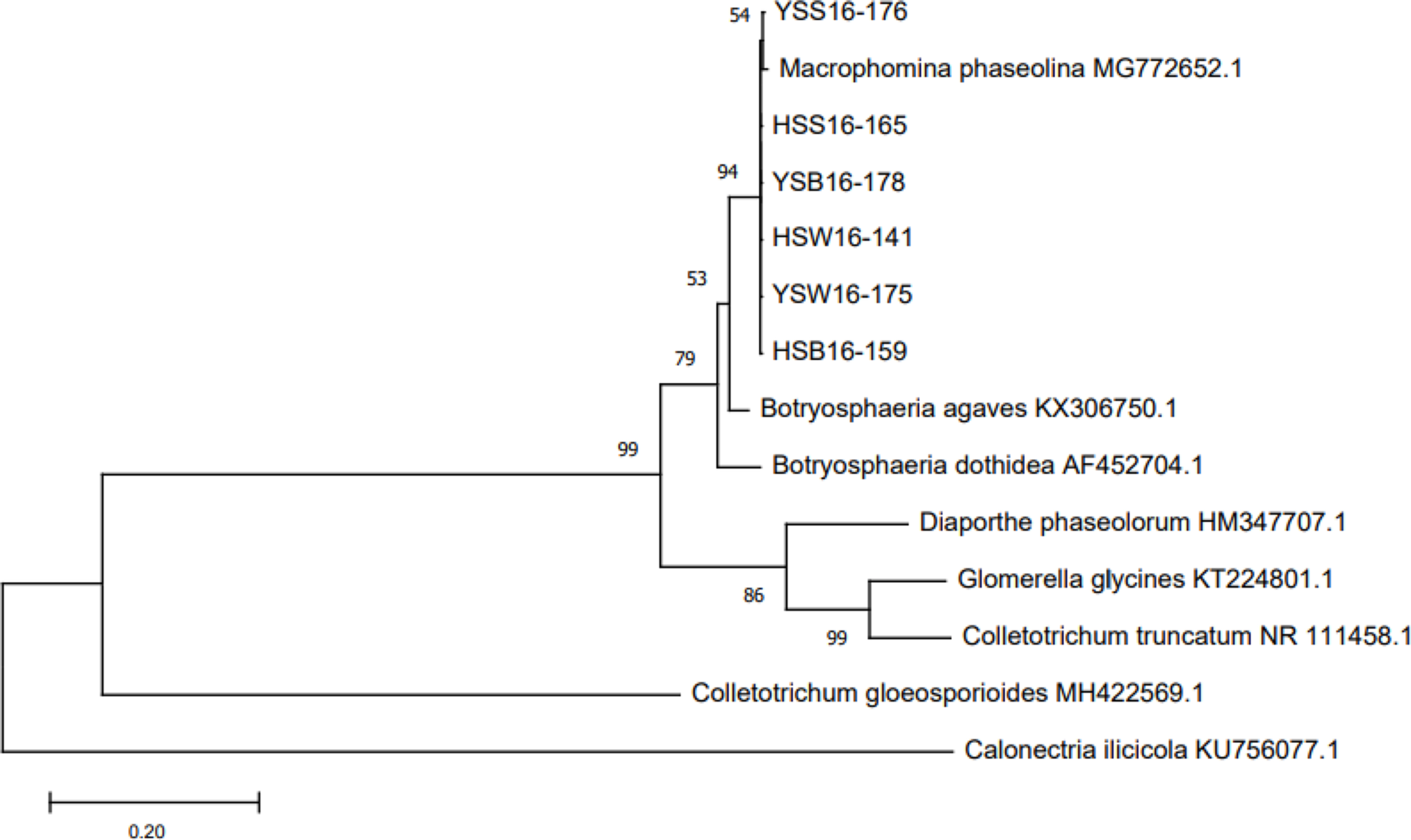
Fig.┬Ā8
Pathogenicity test of Macrophomina phaseolina isolated from infected soybean. (A) Stem blight caused by artificial inoculation of the pathogen, as Macrophomina phaseolina isolated from infected soybean. Left row; non-inoculated soybeans, right row; inoculated soybeans. (B) A typical sign showing macrosclerotia on lesions after an artificial inoculation. (C) The colony of Macrophomina phaseolina reisolated from the symptoms on stems of soybean developed by the artificial inoculation.
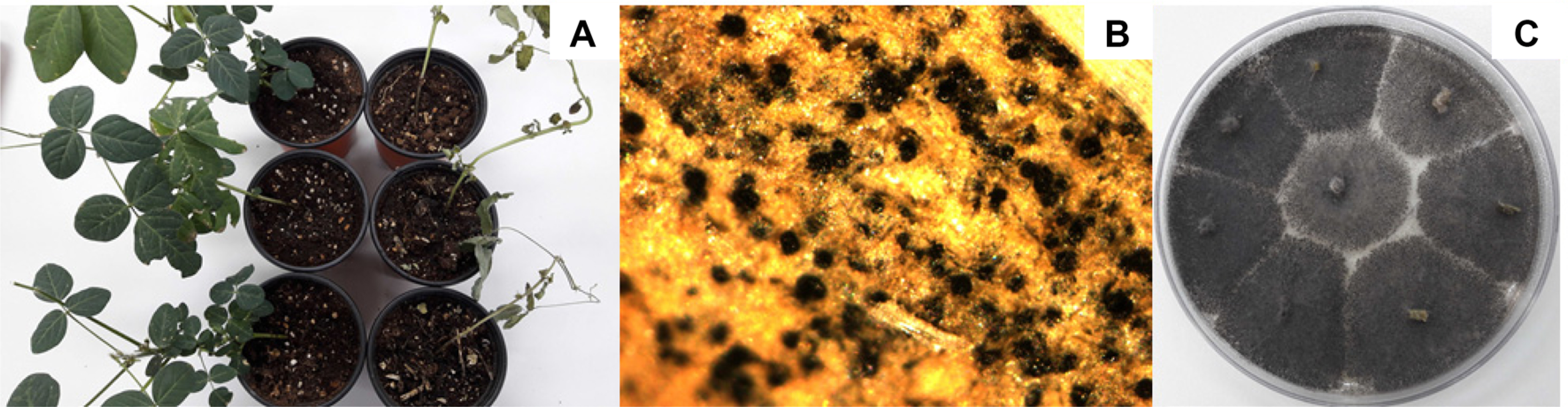
Fig.┬Ā9
Harvested soybeans. Left rows were soybeans harvested from healthy soybeans, and right rows were it from infected soybeans.

Fig.┬Ā10
Effect of the disease caused by Macrophomina phaseolina on the quality of harvested soybeans. (A) Weight of 100 seeds harvested from healthy and infected soybeans. (B) Distribution of soybean grains classified according to the diameter of grains (top, infected seed; B, healthy seed). The weight of 100 seeds was the average of 10 replications. The different letters on the bars are statistically significant based on Duncan multiple range test (PŌēż0.01).
Table┬Ā1
Isolationa of pathogens in several kinds of diseased crop plants collected from the fields
| Pathogens | Soybean | Sesame | Adzuki bean | Mung bean | Peanut | Total |
|---|---|---|---|---|---|---|
| Macrophomina | 16 | 4 | 1 | - b | - | 21 |
| Phomopsis | 40 | 2 | 4 | 1 | 1 | 48 |
| Colletotrichum | 29 | 5 | 3 | 3 | - | 40 |
| Botryospaeria | 11 | 2 | 1 | - | - | 14 |
| Fusarium | - | 1 | - | 1 | - | 2 |
| Other | 9 | 1 | 2 | - | 1 | 13 |
| Total | 105 | 15 | 11 | 5 | 2 | 138 |
References
Allen, T. W., Bradley, C. A., Sisson, A. J., Byamukama, E., Chilvers, M. I., Coker, C. M. et al. 2017. Soybean yield loss estimates due to diseases in the United States and Ontario, Canada, from 2010 to 2014. Plant Health Prog 18: 19-27.
Chidambaram, P. and Mathur, S. B. 1975. Production of pycnidia by Macrophomina phaseolina
. Trans. Br. Mycol. Soc 64: 165-168.

Cummings, J. A. and Bergstrom, G. C. 2013. First report of charcoal rot caused by Macrophomina phaseolina in soybean in New York. Plant Dis 97: 1506

los Santos, B., Aguado, A., Borrero, C., Viejobueno, J. and Avil├®s, M. 2019. First report of charcoal rot, caused by Macrophomina phaseolina, on blueberry in southwestern Spain. Plant Dis 103: 2677

Gogoi, R., Hooda, K. S., Rai, S. N., Kumar, A. and Hossain, F. 2016. Rapid screening technique for evaluation of maize genotypes against stalk rot complex caused by Macrophomina phaseolina and Fusarium verticilloides
. Indian J. Agric. Sci 86: 1024-1030.
Gupta, G. K., Sharma, S. K. and Ramteke, R. 2012. Biology, epidemiology and management of pathogenic fungus Macrophomina phaseolina (Tassi) Goid with special reference to charcoal rot of soybean (Glycine max (L.) Merrill). J. Phytopathol 160: 167-180.

Korea Meteorological Administration. 2020. URL https://data.kma.go.kr/stcs/grnd/grndTaList.do?pgmNo=70
[26 February 2020].
Korean Society of Plant Pathology. 2009. List of Plant Disease in Korea. 5th ed. Korean Society of Plant Pathology, Seoul, Korea. pp. 853 pp.
Korea Statistical Information Service. 2020. URL http://kosis.kr/index/index.do
[26 February 2020].
Short, G. E., Wyllie, T. D. and Bristow, P. R. 1980. Survival of Macrophomina phaseolina in soil and in residue of soybean. Phytopathology 70: 13-17.

Smith, G. S. and Wyllie, T. D. eds. by G. L. Hartman, J. B. Sinclair and J. C. Rupe, 1999. Charcoal rot. In: Compendium of Soybean Diseases, American Phytopathological Society, St. Paul, MN, USA. pp. 29-31.
Sun, S.-L., Zhu, Z.-D., Duan, C.-X., Zhao, P., Sun, F., Deng, D. et al. 2019. First report of charcoal rot caused by Macrophomina phaseolina on faba bean in China. Plant Dis 103: 1415

Sung, J. M., Park, J. H., Lee, S. C. and Chung, B. K. 1980. The outbreak and propagule formation of black root rot caused by Calonectria crotalariae in Korea. Korean J. Plant Prot 19: 228-233. (In Korean)
Kaur, S., Dhillon, G. S., Brar, S. K., Vallad, G. E. and Chauhan, V. B. 2012. Emerging phytopathogen Macrophomina phaseolina: biology, economic importance and current diagenostic trends. Crit. Rev. Microbiol 38: 136-151.


Twizeyimana, M., Hill, C. B., Pawlowski, M., Paul, C. and Hartman, G. L. 2012. A cut-stem inoculation technique to evaluate soybean for resistance to. Macrophomina phaseolina. Plant Dis 96: 1210-1215.
Wrather, J. A., Anderson, T. R., Arsyad, D. M., Gai, J., Ploper, L. D., Porta-Puglia, A. et al. 1997. Soybean disease loss estimates for the top 10 soybean producing countries in 1994. Plant Dis 81: 107-110.


Yu, S. H. 1980.
Macrophomina phaseolina detected in seeds of Sesamum indicum and it's pathogenicity. Plant Prot 19: 135-140.
Yu, S. H. and Park, J. S. 1982. Survey on seed-borne fungi in some important crops of Korea. Res. Rep. Agric. Sci. Technol. Chungnam Natl. Univ 9: 275-283. (In Korean)
Yum, K. J. and Park, E. W. 1989. Occurrence and distribution of soybean seed-borne fungi in Korea. Korean J. Plant Pathol 5: 287-293. (In Korean)
- TOOLS
-
METRICS

- Related articles
-
First Report of Soft Rot Induced by Dickeya dadantii on Euphorbia hypogaea in Korea2024 March;30(1)



 PDF Links
PDF Links PubReader
PubReader Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print