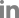분리균의 탄소원 이용 여부를 조사하기 위하여 TSA (Tryptic Soy Agar)에서 2일 배양한 신선한 콜로니를 면봉으로 채취하여 Inoculating fluid 용액에 현탁하고, Biolog 전용 탁도계를 이용하여 농도를 조절 한 후, GEMIII Microplate (BiologInc., Hayword, Co., USA)에 100 ul씩 분주하여 28°C에서 배양하였다. 24시간 배양 후, MicroLog™3-Automated Microstation System을 이용하여 탄소원 이용 여부를 조사하고, MicroLog Gram-negative database(Version 4.02)와 연결하여 동정하였다. 미생물의 탄소원 및 생화학 특성을 분석하는 Biolog system을 이용하여 동정한 결과
Serratia plymuthica로 85% 유사도, 100%의 가능성으로 동정되었다. 사용하는 탄소원은 Dextrin 등 27개이고 화학물질에 대해서 pH 6 산도에서의 생장, 1% NaCl, 1% Sodium Lactate, Troleandomycin, Rifamycin SV, Lincomycin, Niaproof 4, Vancomycin, Tetrazolium Blue에 양성을 나타내었고, pH 5, 4% NaCl, 8% NaCl, Nalidixic Acid, Fusidic Acid 등에는 음성을 보였다(
Table 1). 세균의 생화학적 특성 분석을 위하여 Vitek 2 compact(bioMe’ rieux, France) system을 이용하여 분석하였다. 먼저 TSA에 순수 배양된 세균 콜로니를 5×1 cm 튜브에 0.45% NaCl을 3 ml을 분주한 후 Vitek 전용 탁도계인 Densicheck(bioMe’ rieux, France)를 이용하여 탁도 0.6±0.05 Mcfarland로 현탁하였다. 현탁된 균액은 Vitek 전용 rack에 고정 후 GN card에 현탁액을 충진하였다. 충진부터 이하 일련의 과정은 제조사에서 제공한 실험 방법에 따랐다. Vitek 2 system을 통한 생화학적 반응 결과
S. plymuthica로 99% 동정되었으며, L-Pyrrolydonyl-Arylamidase, β-N-Acetylglucosaminidase, Glutamyl-Arylamidase pNA, γ-Glutamyl Transferase, β-Glucosidase, β-Xylosidase, β-Alanine Arylamidase, Lipase, Sucrose, D-Trehalose에 양성을 보였다(
Table 1). 세균의 지방산 분석을 통한 세균 동정 장치인 GC-MIDI를 이용하여 세균을 동정하였다. 세균은 TSA 배지에서 2일간 28°C에서 배양하였다. 세균 콜로니를 1 ml의 saponification reagent (NaOH aqueous methanol)에 첨가하고, 100°C 항온수조에서 30분 간 열을 가한 후, Methylation reagent (hydrochloric acid in aqueous methanol)를 첨가하였다. 지방산은 solvent (hexane/MEBE), mild base (10.8 g NaOH in 900 ml), 그리고 saturated NaOH solution에 의해 추출하였다. 지방산 조성 분석은 Sherlock system을 이용하였으며, MIDI database에 따라 유사도를 측정하였다(MIDI Library version, TSBA 4.0, Library Generation system software version 4.0). 동정 결과
S. plymuthica로 89% 동정되었다. 세균의 16S rDNA 염기서열 분석을 위하여 genomic DNA를 Promega DNA extraction Kit을 이용하여 추출하였고 16S rDNA의 PCR 증폭을 위해 27F (5’-AGAGTTTGATCMTGGCTCAG-3’)와 1492R (5’-GGYTACCTTGTTACGACTT-3’)의 primer를 사용하였다. PCR 반응 조건은 predenaturation(60°C, 2분), denaturation (98°C, 1분), annealing (60°C, 1분), extension (72°C, 1분), total cycle (30 cycle), final extension (72°C, 4분)이었으며, 증폭된 PCR 산물은 1% agarose gel, 0.5 X TBE buffer (0.045 M Tris-borate, 0.001 M EDTA)에서 100 V, 25 mA로 30분 전기영동 후 UV 하에서 확인하였다. PCR 산물을 DNA 염기서열 분석 전문 업체(Solgent, Daejeon, Korea)에 의뢰하였으며, Seqman (DNASTAR, USA) 프로그램을 이용하여 분석하였다. DNASTAR program을 이용하여 염기서열을 붙여 완성한 후 Phylogenetic tree를 작성하고 NCBI (National Center for Biotechnology Information)의 BLAST search를 이용하여 Genbank에 등록되어 있는 균주들과 유사도를 조사하였다. 이세균의 16S rRNA의 염기서열을 분석한 결과,
Serratia plymuthica strains와 99.0-99.9%의 homology를 나타냈다(
Fig. 5).
Serratia 속 세균이 인삼의 뿌리썩음병을 유발시키는 종으로는
Serratia liquefaciens가 보고되었다.
Serratia liquefaciens를 인삼 뿌리에 인공 접종하였을 때, 잎은 황화되거나 검은색으로 변하여 시들고 줄기는 속이 썩어 텅 비게 되며, 뿌리는 접종부위가 썩으면서 주름이 생기고 차츰 검은색으로 변한다(
Kim 등, 2004). 2011년 폴란드에서 Kowalska 등이 양파 구근에서 이 병원균에 의해 구근썩음병을 일으킨다고 보고 된 바 있다(
Kowalska 등, 2011). 따라서
Serratia 속 세균이 인삼의 뿌리썩음 증상을 유발하는 병원성 세균이 존재하는 것으로 보인다. 그러나
Serratia marcescens는 사과 푸른곰팡이병 방제를 위하여 처리하였을 때, 48%의 방제효과가 있다고 보고되었다(
Kim 등, 2003).
S. plymuthica를 양파 근권에서 분리하여 배양 후, 하우스 내에서 고추 역병에 방제효과가 있는 것으로 보고하였다(
Shen 등, 2002,
2005,
2007).
S. plymuthica이 생산하는 역병의 포자발아 억제물질은 macrocyclic lactone A21-4으로 밝혀졌다(
Shen 등, 2007). 토양 온도가 20°C, 토양 pH가 중성이거나 약산성토양이
S. plymuthica A21-4의 근권정착에 유리하였으며, 살균한 토양보다 토착미생물이 있을 때 토양에 더 잘 정착한다고 하였다(
Pu, 2009). 본 연구에서
S. plymutica는 인삼에서 뿌리썩음병을 유발하는 병원균으로 증명되었으며 인삼 세균뿌리썩음병(Bacterial root rot on ginseng)으로 보고한다. 따라서
Serratia plymuthica strain을 인삼에 생물학적 방제제로 적용하는 경우 사용에 주의를 기울여야 할 것이며, 추후 일부 작물에 길항미생물로 경작지에 사용되고 있는
S. plymuthica strain과의 유전적, 생물학적 특성 비교를 수행하여야 할 것으로 생각된다. 이 병은 일반적인 식물세균병과 마찬가지로 토양수분이 과습한 환경에서 다발생하는 것으로 보인다. 차광망 시설에 구멍이 나거나 문제가 있어 빗물이 다량 유입된 두둑 주변의 인삼이 집중적으로 감염되는 것으로 관찰되었다. 차광망을 정상적으로 보수하여 빗물이 누수되지 않도록 하여야 이 병에 의한 피해를 줄일 수 있다.






 PDF Links
PDF Links PubReader
PubReader Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print